血管生成素系统由血管生成素(Angiopoietin,Ang)和其酪氨酸激酶受体Tie-2组成,Ang包括Ang-1、Ang-2、Ang-3、Ang-4,其中研究比较多的是Ang-1和Ang-2[1 。Ang-1由肝星状细胞分泌,主要功能是促进血管生长和稳定,抑制炎症,促进内皮细胞存活[2 。相反,Ang-2由血管内皮细胞分泌,主要功能是促进血管的活化和炎症反应,拮抗Ang-1的作用[3 。由于Ang-1和Ang-2是拮抗配体,因此Ang-1/Ang-2比值反映了它们之间的不平衡,与疾病进展和预后相关[4 。血管生成素系统主要涉及血管稳定和炎症反应,已经有许多疾病将其作为疾病严重程度及预后的靶标,如糖尿病、结核、败血症等[5 6 。但在慢性乙型肝炎(CHB)、肝硬化研究方面,尚未见报道。
1.
资料与方法
1.1
研究对象
选取首都医科大学附属北京佑安医院2018年3月—2019年10月收治的CHB、乙型肝炎肝硬化患者,收集临床资料和血清标本;另选同期健康体检者作为对照组。纳入标准:(1)CHB和肝硬化诊断符合《慢性乙型肝炎防治指南(2019年版)》[7 ;(2)既往无抗病毒治疗史,初治,未曾进行抗纤维化干预。排除标准:(1)合并甲、丙、丁、戊型肝炎,药物性肝炎、非酒精性脂肪性肝病、酒精性肝病及自身免疫性肝病;(2)合并糖尿病、结核、肾病、血管疾病等;(3)明确诊断的肝癌患者;(4)临床资料缺失或检查不完善的患者。
1.2
研究方法
1.2.1
PCR法定量检测HBV DNA
采用罗氏Light Cycler 480检测仪,试剂盒采用中国圣湘生物科技股份有限公司的HBV DNA试剂盒,检测灵敏度为100 IU/mL。
1.2.2
血生化检验
入组患者均禁食12 h后采静脉血,采用日本Olympus AU 2700全自动生物化学仪器检测ALT水平。
1.2.3
ELISA 方法检测血清Ang-1、Ang-2水平
采用R & D试剂盒,操作方法按照试剂盒说明书。
1.3
统计学方法
应用SPSS 17.0统计学软件进行数据分析。正态分布的计量资料以x ¯ s 表示,非正态分布的计量资料以M (P 25 ~P 75 )表示,多组间比较采用Kruskal-Wallis H 检验,进一步两两比较采用Bonferroni法;相关性分析采用Spearman法。P <0.05为差异有统计学意义。
2.
结果
2.1
一般资料
本研究共纳入患者158例,其中CHB组99例,男57例,女42例,平均年龄为(47.62±8.34)岁,平均病程为(8.95±2.13)年;肝硬化组59例,男39例,女20例,平均年龄为(59.36±7.21)岁,平均病程为(13.57±5.72)年。对照组46例,男24例,女22例,平均年龄为(45.15±7.28)岁。
2.2
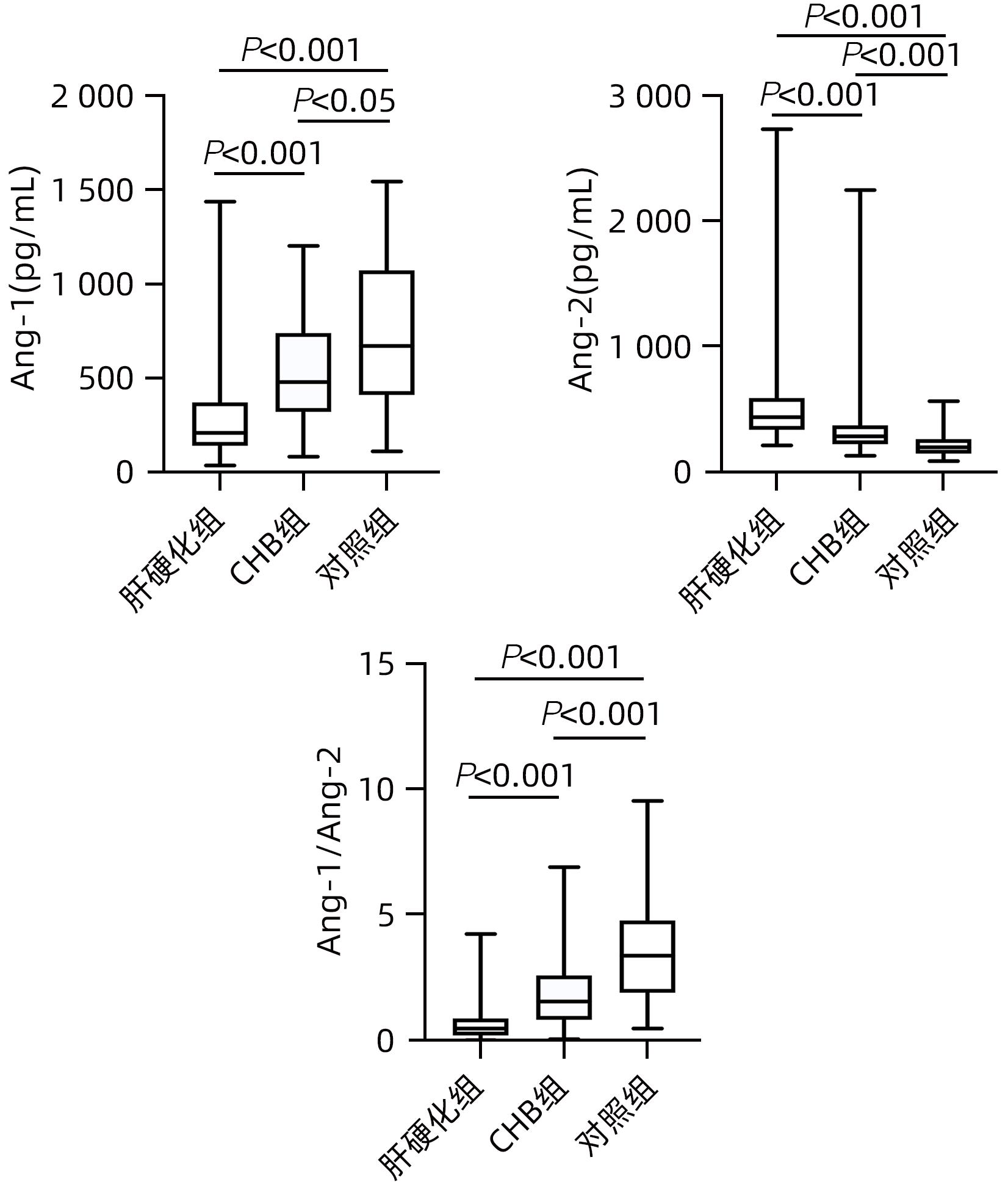
各组血清Ang-1、Ang-2表达水平及Ang-1/Ang-2比值比较
与对照组比较,CHB组和肝硬化组Ang-1水平均降低(P 值均<0.05);与CHB组相比,肝硬化组Ang-1水平降低(P <0.001)。与对照组比较,CHB组和肝硬化组Ang-2水平均升高(P 均<0.001);与CHB组相比,肝硬化组Ang-2水平升高(P <0.001)。与对照组比较,CHB组和肝硬化组Ang-1/Ang-2的比值均降低(P 值均<0.001);与CHB组相比,肝硬化组Ang-1/Ang-2的比值降低(P <0.001)(表1 图1
2.3
CHB组和肝硬化组Ang-1、Ang-2及Ang-1/Ang-2比值与HBV DNA、ALT的相关性分析
CHB组及肝硬化组患者血清HBV DNA分别为3.78(1.91~6.01)、1.67(1.52~2.61) IU/mL,ALT分别为52.50(25.25~121.15)、26.00(18.60~41.10)U/L。Spearman相关分析结果显示,在CHB组,Ang-1与HBV DNA及ALT均呈负相关(P 值均˂0.001);Ang-2与HBV DNA及ALT均呈正相关(P 值均˂0.001);Ang-1/Ang-2与HBV DNA及ALT均呈负相关(P 值均˂0.001)(表2 P 值均˃0.05)(表3
3.
讨论
CHB、肝硬化的进展伴随着血管反应,研究[8 11 报道,血管生成素系统涉及感染性疾病、纤维化以及肿瘤等,但在CHB、肝硬化方面还未见报道。
Jeansson等[2 报道在组织损伤后,Ang-1在减轻组织损伤、减慢血管生成和纤维化方面发挥重要作用。Saharinen等[12 报道Ang-1的补充使各种小鼠疾病模型中的血管功能正常化,如减轻氧诱导的视网膜病变、脉络膜新生血管、糖尿病肾病、全身炎症、败血症和心脏同种异体移植的排斥反应。本研究显示,CHB组和肝硬化组与对照组比较,Ang-1的表达显著降低,表明其对肝组织的保护作用明显减弱,或许预示该患者肝组织损伤及炎症反应比较严重,且预后不良。
另有研究[13 19 报道,许多与血管功能失调相关的疾病,如败血症、癌症、糖尿病、严重创伤、疟疾和病毒性出血热中,Ang-2均显著增加。过多分泌的Ang-2破坏了血管内皮细胞的连接,导致大量的血浆渗出,血管异常增生;还可以增加血管内皮细胞对血管生长因子、致炎因子的敏感性[13 20 。本研究中,CHB组和肝硬化组与对照组比较,Ang-2的表达显著增加,拮抗Ang-1对肝组织及血管内皮细胞的保护作用,可能进一步加重了肝组织的损伤、炎症反应,甚至纤维化。
已有研究[5 21 22 报道,将Ang-2及Ang-2/Ang-1比值作为疾病严重程度、预后及治疗效果的生物标志物。本研究观察到,CHB、肝硬化患者血清Ang-1、Ang-2及Ang-1/Ang-2有显著改变,其中肝炎组Ang-1、Ang-2及Ang-1/Ang-2与HBV DNA和ALT有相关性。CHB组和肝硬化组与对照组相比,Ang-1/Ang-2比值显著降低。Ang-1和Ang-2是相互拮抗、相互制约的关系,笔者认为不论Ang-1或Ang-2增加或减少,只要其比值在正常范围,表明肝组织的损伤及炎症反应就相对比较轻微;反之,当Ang-2显著增加,Ang-1不增反降,Ang-1/Ang-2比值明显降低时,表明炎症反应比较重,预后不良。
综上所述,在CHB阶段Ang-1、Ang-2及Ang-1/Ang-2比值与患者HBV感染及肝损伤程度相关,或许可作为指导CHB治疗和预测CHB患者预后的临床指标之一。








 下载:
下载:






 DownLoad:
DownLoad: