γ链细胞因子对慢性乙型肝炎患者T淋巴细胞免疫球蛋白黏蛋白分子3表达调控的诱导机制
DOI: 10.3969/j.issn.1001-5256.2021.05.017
Mechanism of gamma-chain cytokines in regulating the expression of T-cell immunoglobulin and mucin domain-containing molecule 3 in CD8+ T cells of chronic hepatitis B patients
-
摘要:
目的 探讨γ链(γC)细胞因子对慢性乙型肝炎(CHB)患者CD8+T淋巴细胞中T淋巴细胞免疫球蛋白黏蛋白分子3(TIM-3)表达调控的机制。 方法 选取2017年1月—5月在第四军医大学唐都医院就诊的CHB患者23例,采集外周血,利用Ficoll密度梯度离心法分离外周血单个核细胞,分别使用IL-7、IL-15和IL-21刺激培养,同时向培养液中加入抗γC和/或抗IL-7Rα、抗IL-2Rβ、抗IL-21R。培养96 h后,流式细胞术检测CD8+T淋巴细胞中TIM-3表达水平以及IL-2、IL-10、IFNγ和相关磷酸化信号传导及转录激活蛋白(STAT)磷酸化水平。计量资料多组间比较采用单因素方差分析,进一步两两比较采用LSD-t检验。 结果 IL-7和IL-15刺激后,CD8+T淋巴细胞中TIM-3阳性细胞比例较无刺激组升高(t值分别为9.966、9.074,P值均<0.05),IL-2、IL-10、IFNγ水平以及STAT-5、pSTAT-1水平亦较无刺激组升高(P值均<0.05)。抗IL-7Rα+抗γC联合刺激后可降低IL-7刺激组TIM-3、IL-2和IL-10表达升高(t值分别为5.537、6.224和4.500,P值均<0.05)。抗IL-2Rβ单独刺激、抗IL-2Rβ+抗γC刺激均可降低IL-15刺激组的TIM-3、IL-2、pSTAT-1水平(P值均<0.05)。 结论 IL-7和IL-15可能主要通过γC受体介导的STAT-细胞因子信号通路上调CHB患者CD8+T淋巴细胞中TIM-3表达。 -
关键词:
- 乙型肝炎, 慢性 /
- 细胞因子类 /
- CD8阳性T淋巴细胞 /
- T淋巴细胞免疫球蛋白黏蛋白分子3
Abstract:Objective To investigate the mechanism of gamma-chain (γC) cytokines in regulating the expression of T-cell immunoglobulin and mucin domain-containing molecule 3 (TIM-3) in CD8+ T cells of chronic hepatitis B (CHB) patients. Methods A total of 23 CHB patients who attended Tangdu Hospital, Fourth Military Medical University, from January to May, 2017, were enrolled. Peripheral blood was collected from all patients, and Ficoll density gradient centrifugation was used to isolate peripheral blood mononuclear cells (PBMCs). PBMCs were stimulated with interleukin-7 (IL-7), interleukin-15 (IL-15), and interleukin-21, respectively, and then anti-γC antibody and/or anti-IL-7Rα, anti-IL-2Rβ, and anti-IL-21R were added to the culture solution. After 96 hours of culture, flow cytometry was used to measure the expression of TIM-3, interleukin-2 (IL-2), interleukin-10 (IL-10), and interferon-γ (IFNγ) and the phosphorylation level of signal transducer and activator of transcription (STAT) in CD8+ T cells. A one-way analysis of variance and the least significant difference t-test were used for comparison of continuous data. Results The CD8+ T cells stimulated by IL-7 and IL-15 had a significantly higher percentage of TIM-3-positive CD8+ T cells than those without stimulation (t=9.966 and 9.074, P < 0.05), as well as significantly higher expression levels of IL-2, IL-10, and IFN-γ and phosphorylation levels of STAT-5 and STAT-1 (all P < 0.05). Stimulation with anti-IL-7Rα and anti-γC antibody significantly reduced the elevated expression levels of TIM-3, IL-2, and IL-10 in the IL-7 stimulation group (t=5.537, 6.224, and 4.500, P < 0.05). Stimulation with anti-IL-2Rβ alone or in combination with anti-γC antibody significantly reduced the expression levels of TIM-3 and IL-2 and the phosphorylation level of STAT-1 in the IL-15 stimulation group (P < 0.05). Conclusion IL-7 and IL-15 can upregulate the expression of TIM-3 in CD8+ T cells of CHB patients, possibly via the γC receptor-mediated STAT-cytokine signaling pathway. -
γ链(γ chain, γC)细胞因子家族成员包括IL-2、IL-4、IL-7、IL-9、IL-15和IL-21,受体为γC受体亚基和特异性α/β受体亚基形成的异源二聚体,在慢性病毒感染过程中调控CD4+T淋巴细胞和CD8+T淋巴细胞功能,影响机体抗病毒免疫活性[1-2]。T淋巴细胞免疫球蛋白黏蛋白分子3(T-cell immunoglobulin and mucin domain-containning molecule 3, TIM-3)是重要的免疫检查点分子,主要发挥负性调控机体免疫应答的作用[3]。在人免疫缺陷病毒(HIV)感染中,γC细胞因子可诱导CD8+T淋巴细胞中TIM-3表达升高,通过相应异源二聚体受体介导的信号通路影响下游细胞因子分泌[4]。本课题组前期研究[5-6]也发现,慢性乙型肝炎(CHB)患者外周血CD4+T淋巴细胞和CD8+T淋巴细胞中TIM-3表达升高,IL-7和IL-15可增强CHB患者CD8+T淋巴细胞中TIM-3的表达,但抑制γC受体亚基并不影响IL-7和IL-15诱导的TIM-3表达升高。因此,本研究通过抑制CD8+T淋巴细胞中各种γC细胞因子受体特异性α/β亚单位,探讨γC细胞因子诱导CD8+T淋巴细胞中TIM-3表达调控的机制。
1. 资料与方法
1.1 研究对象
选取2017年1月—5月就诊于第四军医大学唐都医院传染科的CHB患者。纳入标准:(1)符合《慢性乙型肝炎防治指南(2015更新版)》[7]的诊断标准;(2)年龄≥18岁;(3)获得知情同意。排除标准:(1)近1年内曾接受抗病毒治疗或免疫调节治疗者;(2)合并其他嗜肝病毒或HIV感染者;(3)合并自身免疫性疾病、酒精性肝炎、药物性肝损伤者;(4)合并恶性肿瘤者;(5)合并终末期肝脏疾病(包括失代偿期肝硬化、肝衰竭、肝癌)者。
1.2 实验方法
1.2.1 主要试剂和仪器
淋巴细胞分离液购自美国Sigma公司。小鼠抗人CD3-APC、小鼠抗人CD8-FITC、小鼠抗人TIM-3-PE CF594、小鼠抗人磷酸化信号传导及转录激活蛋白-1(signal transducer and activator of transcription-1, STAT-1)-PE(磷酸化位点为Y701)、小鼠抗人磷酸化STAT-3-PerCP Cy5.5(磷酸化位点为Y705)、小鼠抗人磷酸化STAT-5-APC(磷酸化位点为Y694),大鼠抗人IL-2-APC、小鼠抗人IFNγ-FITC、大鼠抗人IL-10-PE购自美国BD公司。重组人IL-7、重组人IL-15、重组人IL-21购自美国PeproTech公司。抗人IL-7Rα、抗人IL-2Rβ、抗人IL-21R、抗γC抗体购自美国R&D公司。流式细胞仪FACS Aria Ⅱ为美国BD公司产品。
1.2.2 外周血单个核细胞(PBMC)的分离
于清晨、空腹采集外周静脉血20 ml,采用EDTA抗凝,立即使用淋巴细胞分离液、采用Ficoll密度梯度离心法分离PBMC。使用0.4%台盼兰对PBMC计数,以5×106个/管分装在冻存管内,加冻存液(90%胎牛血清+10%二甲基亚砜)保存于液氮中备用。
1.2.3 PBMC刺激培养
复苏冻存的PBMC,于24孔板中培养,每孔中加入2×105个PBMC,每例患者设立20个复孔,每2个复孔设立同一刺激因素,分别为:(1)阴性对照(无刺激);(2)重组人IL-7;(3)重组人IL-7+抗人IL-7Rα;(4)重组人IL-7+抗人IL-7Rα+抗γC;(5)重组人IL-15;(6)重组人IL-15+抗人IL-2Rβ;(7)重组人IL-15+抗人IL-2Rβ+抗γC;(8)重组人IL-21;(9)重组人IL-21+抗人IL-21R;(10)重组人IL-21+抗人IL-21R+抗γC,其中重组人IL-7、重组人IL-15、重组人IL-21的终浓度为25 ng/ml,抗人IL-7Rα、抗人IL-2Rβ、抗人IL-21R和抗γC的终浓度为10 μg/ml。PBMC在5% CO2条件下培养90 h,然后加入终浓度为10 μg/ml的布雷菲尔德菌素A继续培养6 h,进行后续实验。
1.2.4 流式细胞检测CD8+T淋巴细胞中TIM-3表达和细胞因子的分泌
刺激后的PBMC转入2个FACS管中,一管加入抗CD3、抗CD8、抗TIM-3、抗pSTAT-1(或抗pSTAT-3、抗pSTAT-5),另一管中加入抗CD3、抗CD8、抗IL-2、抗IL-10、抗IFNγ,并设立同型对照。用FACS Aria Ⅱ流式细胞仪检测,BD FACS Diva软件获取细胞,FlowJo V10软件分析结果。
1.3 伦理学审查
本研究方案经空军军医大学第二附属医院(第四军医大学唐都医院)医学伦理委员会批准,批号:TDLL-201505-013,所有入组志愿者均签署知情同意书。
1.4 统计学方法
采用SPSS 19.0统计软件处理数据。符合正态分布的计量资料使用x±s表示,多组间比较采用单因素方差分析,进一步两两比较采用LSD-t检验。P<0.05为差异有统计学意义。
2. 结果
2.1 一般资料
共纳入CHB患者23例,男14例,女9例,年龄18~41岁,ALT 93~337 U/L,HBV DNA(5.91±1.17)log10IU/ml。
2.2 IL-7对CHB患者CD8+T淋巴细胞中TIM-3、细胞因子和pSTAT-5表达的影响
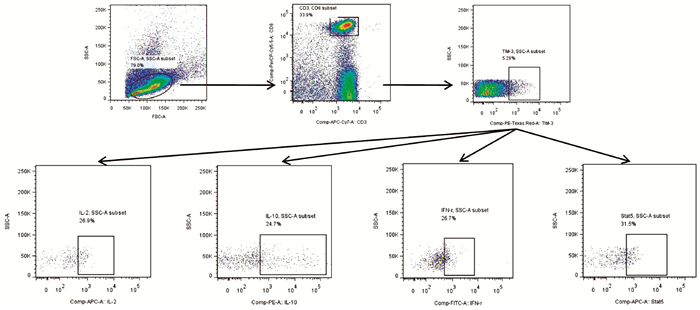
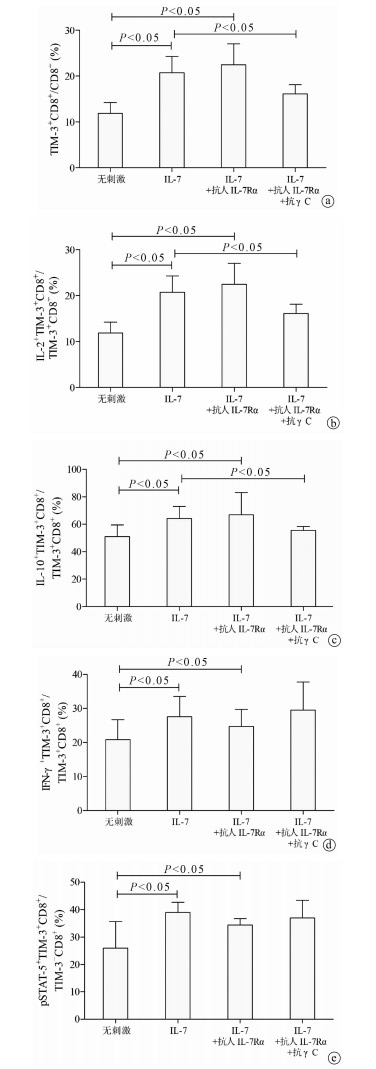
CHB患者CD8+T淋巴细胞中TIM-3和细胞因子分泌、下游pSTAT检测的典型流式分析(图 1)。首先利用前向角散射(forward scatter, FSC)和侧向角散射(side scatter, SSC)对淋巴细胞进行圈门,在淋巴细胞中选择CD3+CD8+T淋巴细胞,检测CD3+CD8+T淋巴细胞中TIM-3+比例,进一步对CD3+CD8+TIM-3+细胞中IL-2、IL-10、IFNγ和pSTAT的比例进行检测。重组人IL-7刺激可诱导CHB患者CD8+T淋巴细胞中TIM-3阳性细胞比例较无刺激组升高[(20.73±3.56)% vs (11.90±2.32)%,t=9.966,P<0.001],亦可诱导TIM-3+CD8+细胞中IL-2阳性[(34.87±10.02)% vs(17.89±6.22)%,t= 6.905,P<0.001]、IL-10阳性[(64.22±8.71)% vs (51.14±8.31)%,t=5.211,P<0.001]、IFNγ阳性[(27.52±5.94)% vs (20.90±5.78)%,t=3.831,P<0.001]细胞比例较无刺激组升高,pSTAT-5阳性细胞比例亦较无刺激组升高[(38.92±3.67) % vs (25.93±9.68)%,t=6.018,P<0.001]。抗人IL-7Rα刺激对IL-7刺激组的TIM-3、IL-2、IL-10、IFNγ和pSTAT-5表达均无显著影响(P值均>0.05)。抗人IL-7Rα和抗γ C联合刺激后可降低IL-7刺激组的TIM-3(16.10±2.01)%、IL-2(18.01±8.27)%和IL-10(55.61±2.89)%表达水平(P值均<0.05),但对IFNγ和pSTAT-5表达无显著影响(P值均>0.05)(图 2)。
2.3 IL-15对CHB患者CD8+T淋巴细胞中TIM-3、细胞因子和pSTAT-1表达的影响
重组人IL-15刺激可诱导CHB患者CD8+T淋巴细胞中TIM-3阳性细胞比例较无刺激组升高[(23.93±5.92)%,t=9.074,P<0.001],亦可诱导TIM-3+CD8+细胞中IL-2阳性[(37.72±9.28)%,t=8.513,P<0.001]、IL-10阳性[(83.92±6.90)%,t=14.550,P<0.001]、IFNγ阳性[(28.53±5.64)%,t=4.531,P<0.001]细胞比例较无刺激组升高,pSTAT-1阳性细胞比例亦较无刺激组升高[(40.88±3.69)% vs (25.93±9.68)%,t=6.921,P<0.001]。抗IL-2Rβ单独刺激、抗IL-2Rβ和抗γC联合刺激均可降低IL-15刺激组的TIM-3、IL-2、pSTAT-1表达水平(P值均<0.05),但对IFNγ表达无显著影响(P>0.05)(图 3)。
2.4 IL-21对CHB患者CD8+T淋巴细胞中TIM-3、细胞因子和pSTAT-1、pSTAT-3表达的影响
重组人IL-21刺激、抗IL-21R单独刺激、抗IL-21R和抗γC联合对CHB患者CD8+T淋巴细胞中TIM-3阳性细胞比例、TIM-3+CD8+细胞中IL-2、IL-10、IFNγ、pSTAT-1及pSTAT-3的表达与无刺激组比较均无统计学差异(P值均>0.05)(表 1)。
表 1 IL-21对CHB患者CD8+T淋巴细胞中TIM-3、IL-2、IL-10、IFNγ、pSTAT-1和pSTAT-3表达的影响项目 无刺激 IL-21 IL-21+抗IL-21R IL-21+抗IL-21R+抗γC F值 P值 TIM-3+CD8+/CD8+(%) 11.90±2.32 12.92±2.94 10.62±4.53 10.67±6.23 1.520 0.215 IL-2+TIM-3+CD8+/TIM-3+CD8+ (%) 17.89±6.22 15.37±2.92 14.57±4.01 14.54±4.09 2.401 0.073 IL-10+TIM-3+CD8+/TIM-3+CD8+ (%) 51.14±8.31 49.17±9.70 50.46±9.25 50.41±9.77 0.180 0.909 IFNγ+TIM-3+CD8+/TIM-3+CD8+ (%) 20.90±5.78 22.11±5.02 24.60±9.01 25.42±9.31 1.753 0.162 pSTAT-1+TIM-3+CD8+/TIM-3+CD8+ (%) 17.30±3.66 20.83±3.81 20.71±6.45 19.92±6.84 2.137 0.101 pSTAT-3+TIM-3+CD8+/TIM-3+CD8+ (%) 8.15±2.37 8.68±2.19 8.36±3.18 8.41±3.09 0.145 0.932 3. 讨论
CD8+T淋巴细胞是清除HBV感染的最主要免疫细胞,但持续HBV感染可通过诱导固有免疫系统功能紊乱、调节性T淋巴细胞水平升高、抑制性免疫应答异常活跃等多种机制影响CD8+T淋巴细胞活性,导致CD8+T淋巴细胞功能衰竭,杀伤活性明显减弱,分泌细胞因子能力降低,进一步诱导HBV感染慢性化[8]。免疫检查点分子是目前免疫治疗的热点之一,针对程序性细胞死亡受体-1(programmed cell death-1, PD-1)、细胞毒性T淋巴细胞相关抗原(cytotoxic T lymphocyte associated antigen 4, CTLA-4)和TIM-3等代表性免疫检查点分子均已成为抗肿瘤和慢性感染免疫治疗的重要靶点[9-10]。PD-1和CTLA-4在急性和慢性病毒性肝炎患者中的表达水平升高:在急性肝炎过程中,PD-1和CTLA-4可抑制CD8+T淋巴细胞的杀伤活性,降低CD8+T淋巴细胞对肝细胞的免疫损伤,发挥免疫保护作用;相反,在慢性肝炎过程中,PD-1和CTLA-4则与T淋巴细胞功能衰竭诱导的持续病毒感染密切相关[11]。本课题组既往研究[5-6]发现,免疫检查点分子家族中的重要成员——TIM-3在CHB患者CD4+和CD8+T淋巴细胞中的水平均显著升高,γC细胞因子中的成员IL-2、IL-7和IL-15均可诱导T淋巴细胞表面TIM-3提升,本研究亦发现相同的结果,且与在慢性HIV感染中研究结果一致[4, 12],说明多种慢性病毒感染中均存在TIM-3升高表达,以TIM-3为代表的免疫检查点分子可能与CD8+T淋巴细胞功能衰竭密切相关,参与病毒感染慢性化。
既往的研究认为γC细胞因子的主要功能为促进炎症应答,虽然这些细胞因子共享γC受体亚基,但特异性α/β受体亚基所介导的信号通路却存在差异。IL-7通过IL-7Rα/γC受体介导下游STAT-5磷酸化,IL-15通过IL-2R/γC受体以及抗原提呈细胞表面的IL-15Rα活化STAT-1介导的信号通路,IL-21通过IL-21R/γC受体介导下游STAT-1、STAT-3磷酸化,调控免疫细胞功能[13-14]。γC细胞因子可调控慢性HBV和HIV感染者T淋巴细胞中TIM-3的表达,在HIV感染者中,IL-2、IL-7、IL-15和IL-21均可上调T淋巴细胞中TIM-3表达[4, 12]。但不同γC细胞因子对CHB患者TIM-3的表达调控却存在差异,IL-7和IL-15可诱导CHB患者CD8+T淋巴细胞中TIM-3表达升高,
虽然IL-21在慢性HBV感染中的表达水平升高,在体内和体外均可介导HBV病毒清除[15-16],但IL-21对CHB患者CD8+T淋巴细胞中TIM-3的表达则无显著影响,这可能与γC细胞因子家族成员介导的下游信号通路不同有关[13-14]。同时,抑制IL-21R和/或γC受体对IL-21介导的CD8+T淋巴细胞中TIM-3的表达变化无影响,提示IL-21对CD8+T淋巴细胞的功能调控可能与其受体的表达水平和功能变化无明显相关性,而深入的机制仍有待进一步研究。
IL-7和IL-15均可显著增加CHB患者CD8+T淋巴细胞中TIM-3表达。IL-7在HCV[17-18]和肝细胞癌[16]患者外周血中的表达水平降低,外源性IL-7可降低肝细胞癌患者CD8+T中PD-1的表达,进而促进CD8+T淋巴细胞功能[19]。外源性IL-15在体内可抑制HBV复制[20],但可上调CD4+T淋巴细胞和CD8+T淋巴细胞中PD-1和TIM-3表达[21]。虽然IL-7和IL-15在慢性HBV感染中的表达谱不同,但IL-7和IL-15究竟发挥免疫增强还是免疫抑制作用尚不清楚。本研究发现,IL-7和IL-15可增强CD8+T淋巴细胞表面TIM-3的表达和下游IL-10的分泌,与CHB患者体内负性免疫调节分子通路的激活密切相关,同时,IL-7和IL-15亦可增强下游IL-2和IFNγ的表达,说明二者亦可能激活了机体的免疫应答。因此,笔者推测,在慢性HBV感染中,以IL-7和IL-15为代表的γC细胞因子不但可诱导TIM-3等负性免疫分子表达,还可促进炎症细胞因子激活,使CD8+T淋巴细胞的增殖和杀伤活性与负性免疫调节在一定范围内达到免疫稳态,使机体既不能清除病毒,也不受到过强的免疫损伤[22]。阻断IL-7和IL-15的特异性受体亚基可降低下游细胞因子的分泌,说明慢性HBV感染者中γC细胞因子可通过与慢性HIV感染者中相似的通路影响下游细胞因子分泌[4, 12]。但由于本研究入组的CHB患者数量有限,且均为体外实验,本研究结果仍需要扩大样本量并以HBV转基因小鼠为研究对象进行体内研究进行进一步确认。
总之,IL-7和IL-15可能主要通过γC受体介导的STAT磷酸化促进细胞因子信号通路,上调CHB患者CD8+T淋巴细胞中TIM-3表达。尽管γC细胞因子被认为是一种治疗慢性病毒感染新的免疫方法,但其具体的治疗机制仍需进一步阐释。
-
表 1 IL-21对CHB患者CD8+T淋巴细胞中TIM-3、IL-2、IL-10、IFNγ、pSTAT-1和pSTAT-3表达的影响
项目 无刺激 IL-21 IL-21+抗IL-21R IL-21+抗IL-21R+抗γC F值 P值 TIM-3+CD8+/CD8+(%) 11.90±2.32 12.92±2.94 10.62±4.53 10.67±6.23 1.520 0.215 IL-2+TIM-3+CD8+/TIM-3+CD8+ (%) 17.89±6.22 15.37±2.92 14.57±4.01 14.54±4.09 2.401 0.073 IL-10+TIM-3+CD8+/TIM-3+CD8+ (%) 51.14±8.31 49.17±9.70 50.46±9.25 50.41±9.77 0.180 0.909 IFNγ+TIM-3+CD8+/TIM-3+CD8+ (%) 20.90±5.78 22.11±5.02 24.60±9.01 25.42±9.31 1.753 0.162 pSTAT-1+TIM-3+CD8+/TIM-3+CD8+ (%) 17.30±3.66 20.83±3.81 20.71±6.45 19.92±6.84 2.137 0.101 pSTAT-3+TIM-3+CD8+/TIM-3+CD8+ (%) 8.15±2.37 8.68±2.19 8.36±3.18 8.41±3.09 0.145 0.932 -
[1] TOE JG, PELLEGRINI M, MAK TW. Promoting immunity during chronic infection—the therapeutic potential of common gamma-chain cytokines[J]. Mol Immunol, 2013, 56(1-2): 38-47. DOI: 10.1016/j.molimm.2013.04.008. [2] TRINITÉ B, CHAN CN, LEE CS, et al. HIV-1 Vpr- and reverse transcription-induced apoptosis in resting peripheral blood CD4 T cells and protection by common gamma-chain cytokines[J]. J Virol, 2016, 90(2): 904-916. DOI: 10.1128/JVI.01770-15. [3] DAS M, ZHU C, KUCHROO VK. Tim-3 and its role in regulating anti-tumor immunity[J]. Immunol Rev, 2017, 276(1): 97-111. DOI: 10.1111/imr.12520. [4] MUJIB S, JONES RB, LO C, et al. Antigen-independent induction of Tim-3 expression on human T cells by the common γ-chain cytokines IL-2, IL-7, IL-15, and IL-21 is associated with proliferation and is dependent on the phosphoinositide 3-kinase pathway[J]. J Immunol, 2012, 188(8): 3745-3756. DOI: 10.4049/jimmunol.1102609. [5] DONG J, YANG XF, WANG LX, et al. Modulation of tim-3 expression by antigen-dependent and -independent factors on T cells from patients with chronic hepatitis B virus infection[J]. Front Cell Infect Microbiol, 2017, 7: 98. DOI: 10.3389/fcimb.2017.00098. [6] DONG J, YANG XF, SHEN HJ, et al. Regulatory effect of gamma-chain cytokines on expression of TIM3 on CD8+ T cells in patients with chronic hepatitis B[J]. J Clin Hepatol, 2015, 31(2): 205-208. DOI: 10.3969/j.issn.1001-5256.2015.02.015.董杰, 杨晓飞, 申焕君, 等. Y链细胞因子对慢性乙型肝炎患者CD8+T细胞上TIM-3表达的调节[J]. 临床肝胆病杂志, 2015, 31(2): 205-208. DOI: 10.3969/j.issn.1001-5256.2015.02.015. [7] Chinese Society of Hepatology and Chinese Socirty of Infectious Diseases, Chinese Medical Association. The guideline of prevention and treatment for chronic hepatitis B: A 2015 update[J]. J Chin Hepatol, 2015, 31(12): 1941-1960. DOI: 10.3969/j.issn.1001-5256.2015.12.002.中华医学会肝病学分会, 中华医学会感染病学分会. 慢性乙型肝炎防治指南(2015更新版)[J]. 临床肝胆病杂志, 2015, 31(12): 1941-1960. DOI: 10.3969/j.issn.1001-5256.2015.12.002. [8] HEIM K, NEUMANN-HAEFELIN C, THIMME R, et al. Heterogeneity of HBV-Specific CD8+ T-Cell failure: Implications for immunotherapy[J]. Front Immunol, 2019, 10: 2240. DOI: 10.3389/fimmu.2019.02240. [9] ZHANG Y, ZHENG J. Functions of immune checkpoint molecules beyond immune evasion[J]. Adv Exp Med Biol, 2020, 1248: 201-226. DOI: 10.1007/978-981-15-3266-5-9. [10] WYKES MN, LEWIN SR. Immune checkpoint blockade in infectious diseases[J]. Nat Rev Immunol, 2018, 18(2): 91-104. DOI: 10.1038/nri.2017.112. [11] CHO H, KANG H, LEE HH, et al. Programmed cell death 1 (PD-1) and cytotoxic T lymphocyte-associated antigen 4 (CTLA-4) in viral hepatitis[J]. Int J Mol Sci, 2017, 18(7). DOI: 10.3390/ijms18071517. [12] ZHANG ZN, ZHU ML, CHEN YH, et al. Elevation of Tim-3 and PD-1 expression on T cells appears early in HIV infection, and differential Tim-3 and PD-1 expression patterns can be induced by common γ -chain cytokines[J]. Biomed Res Int, 2015, 2015: 916936. DOI: 10.1155/2015/916936. [13] LIN JX, LEONARD WJ. The common cytokine receptor γ chain family of cytokines[J]. Cold Spring Harb Perspect Biol, 2018, 10(9): a028449. DOI: 10.1101/cshperspect.a028449. [14] TOE JG, PELLEGRINI M, MAK TW. Promoting immunity during chronic infection—the therapeutic potential of common gamma-chain cytokines[J]. Mol Immunol, 2013, 56(1-2): 38-47. DOI: 10.1016/j.molimm.2013.04.008. [15] SHEN Z, LIU J, WU J, et al. IL-21-based therapies induce clearance of hepatitis B virus persistence in mouse models[J]. Theranostics, 2019, 9(13): 3798-3811. DOI: 10.7150/thno.35331. [16] SHEN Z, WU J, GAO Z, et al. Characterization of IL-21-expressing recombinant hepatitis B virus (HBV) as a therapeutic agent targeting persisting HBV infection[J]. Theranostics, 2020, 10(12): 5600-5612. DOI: 10.7150/thno.44715. [17] ZHANG ZH, JIANG BC, LIU XH, et al. Interleukin-7 regulates T follicular helper cell function in patients with chronic hepatitis C[J]. Viral Immunol, 2018, 31(6): 417-425. DOI: 10.1089/vim.2018.0010. [18] HOU H, KANG Y, ZENG Y, et al. Interleukin-7 augments CD8+ T cells function and promotes viral clearance in chronic hepatitis C virus infection[J]. Cytokine, 2018, 102: 26-33. DOI: 10.1016/j.cyto.2017.12.014. [19] TENG D, DING L, CAI B, et al. Interleukin-7 enhances anti-tumor activity of CD8+ T cells in patients with hepatocellular carcinoma[J]. Cytokine, 2019, 118: 115-123. DOI: 10.1016/j.cyto.2018.04.003. [20] YIN W, XU L, SUN R, et al. Interleukin-15 suppresses hepatitis B virus replication via IFN-β production in a C57BL/6 mouse model[J]. Liver Int, 2012, 32(8): 1306-1314. DOI: 10.1111/j.1478-3231.2012.02773.x. [21] HAKIM MS, JARIAH R, SPAAN M, et al. Interleukin 15 upregulates the expression of PD-1 and TIM-3 on CD4+ and CD8+ T cells[J]. Am J Clin Exp Immunol, 2020, 9(3): 10-21. http://www.researchgate.net/publication/344419769_Interleukin_15_upregulates_the_expression_of_PD-1_and_TIM-3_on_CD4_and_CD8_T_cells [22] PENG H, TIAN Z. NK cells in liver homeostasis and viral hepatitis[J]. Sci China Life Sci, 2018, 61(12): 1477-1485. DOI: 10.1007/s11427-018-9407-2. 期刊类型引用(4)
1. 史雨晨. 免疫球蛋白指标检验对慢性乙型肝炎患者的临床意义. 中国医学创新. 2025(01): 149-152 .  百度学术
百度学术2. 凌珺,朱冰,陈威巍,王卓然,余丽梅,游绍莉. 半乳糖凝集素-9(Gal-9)介导的免疫调节作用在肝脏疾病中的研究进展. 临床肝胆病杂志. 2024(01): 193-198 .  本站查看
本站查看3. 郭静. IL-2、IL-18、IL-21与病毒性肝炎肝硬化合并HIV感染AIDS病情转归相关性研究. 中国现代医药杂志. 2023(01): 64-67 .  百度学术
百度学术4. 徐杨,赵阳,郭慧. 慢性乙型肝炎患者免疫球蛋白检验的临床价值. 中国医药指南. 2022(17): 117-119 .  百度学术
百度学术其他类型引用(0)
-




 PDF下载 ( 3290 KB)
PDF下载 ( 3290 KB)


 下载:
下载:


 下载:
下载:

 百度学术
百度学术




