Further discussion on the antiviral treatment of chronic hepatitis B patients with indeterminate phase
-
摘要: 本文再次探讨不确定期慢性乙型肝炎患者的抗病毒治疗。此类患者的肝脏有显著坏死炎症和纤维化的比例较高,疾病进展的风险高于真正的HBeAg阳性慢性HBV感染(既往称为免疫耐受期)或HBeAg阴性慢性HBV感染(既往称免疫控制期)。对不确定期慢性HBV感染者进行抗病毒治疗可降低HBV相关肝细胞癌的风险。Abstract: This paper discusses further on the antiviral treatment of chronic hepatitis B patients with indeterminate phase. These patients have a high proportion of significant necroinflammation and fibrosis in the liver, and a higher risk of disease progression compared with those with true HBeAg-positive chronic hepatitis B virus (HBV) infection (formerly called the immune tolerance phase) or HBeAg-negative chronic HBV infection (formerly called the immune control phase). Antiviral therapy may reduce the risk of HBV-related hepatocellular carcinoma in chronic hepatitis B patients with indeterminate phase.
-
2022年2月发布的《扩大慢性乙型肝炎抗病毒治疗的专家意见》[1],其推荐意见5是:“对于随访1年以上,HBV DNA和ALT模式难以确定且未经治疗的不确定期慢性乙型肝炎患者,建议抗病毒治疗”。但是,在我国2022年12月发布的《慢性乙型肝炎防治指南(2022年版)》[2](简称中国2022年版指南)中,对不确定期HBV感染者未提出推荐意见,只在文中提及“这部分患者疾病进展风险相对较高,因而可能也需要抗病毒治疗”。
1. 不确定期慢性乙型肝炎客观存在
2008年印度Kumar等[3]最早报告存在不属于慢性HBV感染自然史4个期的患者,在ALT持续正常的HBeAg阳性慢性乙型肝炎患者中占40%;在ALT持续正常的HBeAg阴性慢性乙型肝炎患者中占55%。2014年美国Hsu等[4]正式提出“不确定期慢性HBV感染”一词并报告,该期患者在慢性HBV感染中占33%~37%。2017年欧洲肝病学会(EASL)在“慢性HBV感染管理临床实践指南”[5]中,描述了不确定期慢性HBV感染;2021年北美洲肝病专家组发布的“美国HBV感染管理治疗流程:2021年更新”[6],也有关于不确定期慢性HBV感染的叙述。2022年Choi等[7]将不确定期写入慢性乙型肝炎治疗流程图。2023年Dusheiko等[8]将不确定期列为慢性HBV感染自然史的一个期。据国内外报道,在慢性HBV感染者中,不确定期患者占27.8%~59.5%[9-15](表1)。也有将不确定期称为灰区(gray zone)[9,12-14]。
表 1 慢性HBV感染者中不确定期患者的比例Table 1. The proportion of individuals in the indeterminate phase among patients with chronic HBV infection作者 总例数 不确定期例数 比例(%) 诊断标准 Yao等(2021)[9] 4 759 1 323 27.8 AASLD(2018) Duan等(2021)[10] 327 122 37.3 CSH/CSID(2019) Huang等(2022)[11] 3 366 1 303 38.7 AASLD(2018) Jiang等(2023)[12] 634 377 59.5 CSH/CSID(2019) Wang等(2023)[13] 1 043 242 23.2 AASLD(2018) Xu等(2023)[14] 3 462 1 444 41.7 CSH/CSID(2022) Ju等(2023)[15] 1 544 574 37.2 AASLD(2018) 注:AASLD,美国肝病学会;CSH,中华医学会肝病学分会;CSID,中华医学会感染病学分会。 2. 不确定期慢性HBV感染者有显著肝脏病理学改变的比例较高
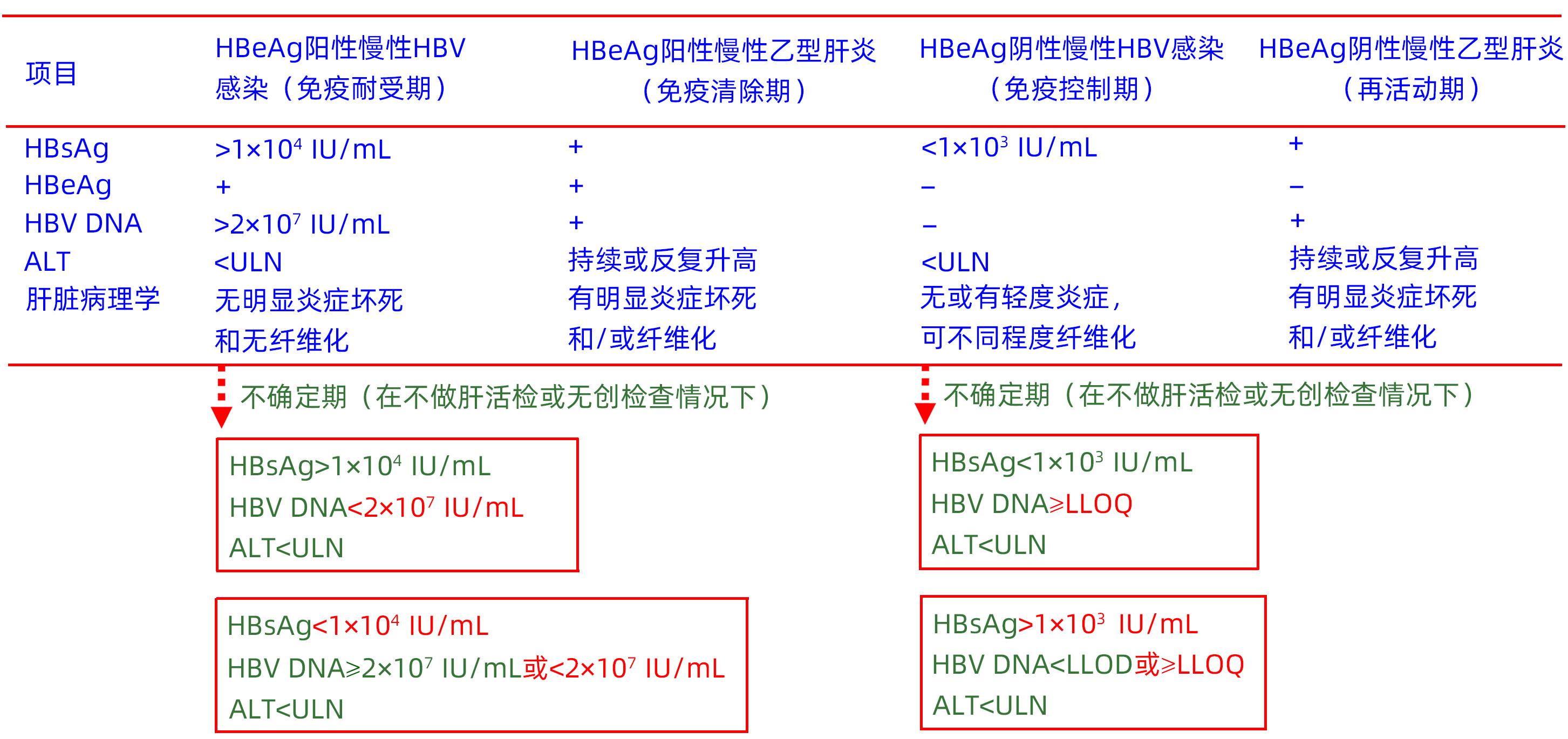
中国2022年版指南的推荐意见10提出,对于血清HBV DNA阳性,ALT持续异常(大于最高值上限),且排除其他原因所致者,建议抗病毒治疗[2]。因此,如按该指南分期,HBeAg阳性和阴性慢性乙型肝炎(既往分别称免疫清除期和再活动期)患者均应接受抗病毒治疗,不存在不确定期患者。但是,在HBeAg阳性和阴性慢性HBV感染(既往分别称免疫耐受期和免疫控制期)患者中,仍有不确定期(图1)。经肝活检证明,在这些不确定期患者中,有显著坏死炎症者占29.2%~84.4%;有显著肝纤维化者占34.0%~73.3%;有显著坏死炎症和/或显著肝纤维化者占49.7%~91.1%[12-13,16](表2),表明多数不确定期患者符合中国2022年版指南推荐的抗病毒治疗标准。
表 2 HBeAg阳性和阴性慢性HBV感染期的不确定期患者肝组织病理学Table 2. Liver histopathology of indeterminate-phase patients with HBeAg-positive and HBeAg-negative chronic HBV infection作者 显著坏死炎症 显著纤维化 显著组织学病变 Liu等(2022)[16] 68.3%(397/581) 58.5%(340/581) 49.7%(289/581) Jiang等(2023)[12] 29.2%(110/377) 34.0%(128/377) 40.6%(153/377) Wang等(2023)[13] HBeAg阳性 84.4%(38/45) 73.3%(33/45) 91.1%(41/45) HBeAg阴性 54.3%(107/197) 53.3%(105/197) 68.5%(135/197) 小计 59.9%(145/242) 57.0%(138/242) 72.7%(176/242) 3. 不确定期患者发生肝细胞癌(HCC)的风险较高
Choi等[17]对3 572例未治疗的非活动期(HBV DNA<2 000 IU/mL,ALT<ULN)和900例未治疗的不确定期(HBV DNA≥2 000 IU/mL,ALT<ULN)患者中位随访8.9年,最长10年,不确定期患者估计的HCC发病率为0.96/100人年,非活动期患者为0.41/100人年,前者显著高于后者(P<0.001)。对273例未治疗的不确定期和治疗的免疫活动期(HBV DNA≥2 000 IU/mL,ALT≥2×ULN)患者进行倾向计分配对分析,未治疗的不确定期患者发生HCC、死亡和肝移植风险比率(hazard ratio,HR)分别为1.76和2.14,显著高于治疗的免疫活动期患者(P=0.049和P=0.03)。
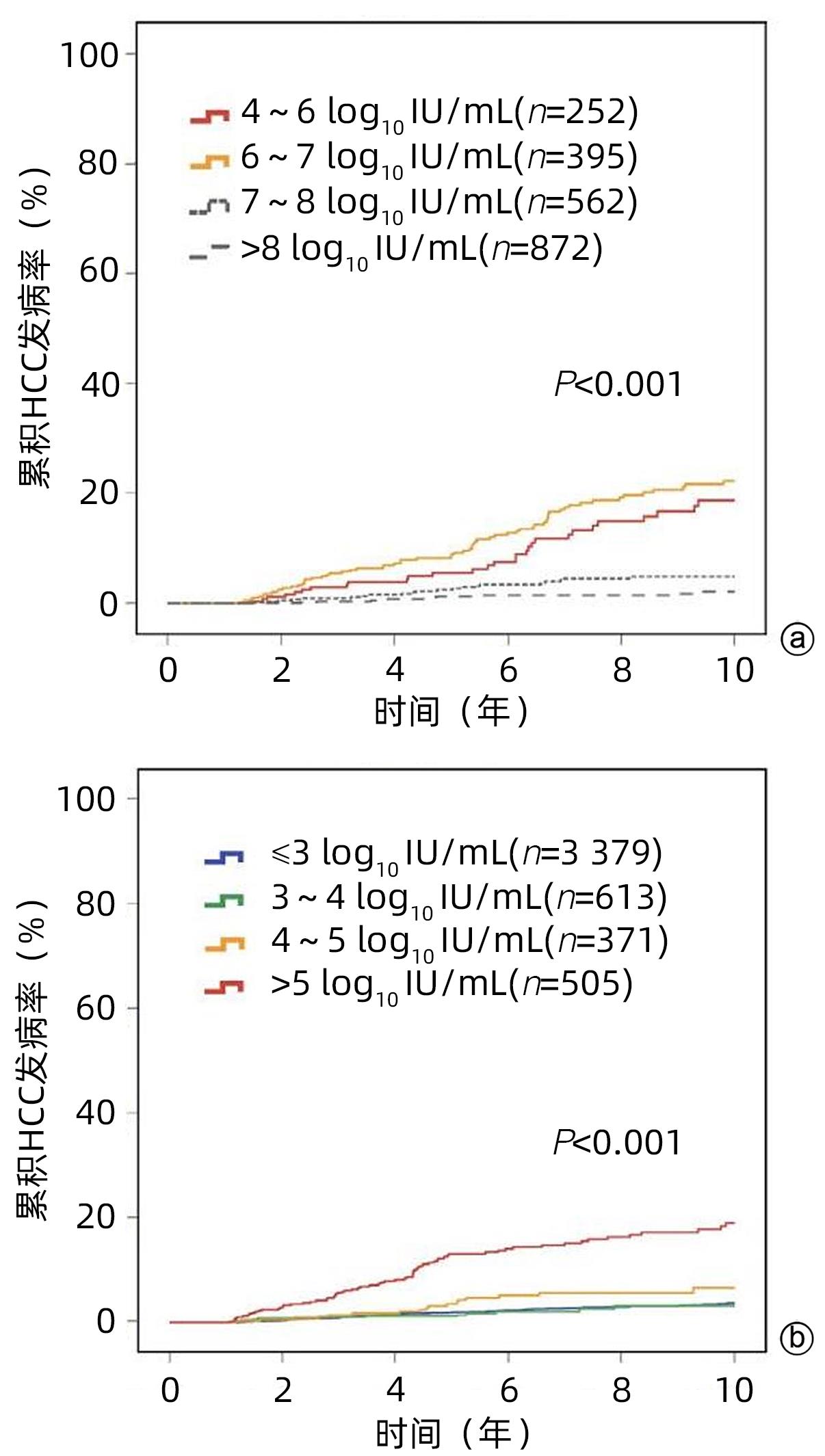
韩国Kim等[18]分析6 949例无肝硬化、初治、ALT<2×ULN至少1年患者的历史队列(2 029例HBV DNA>6 log10 IU/mL),其中HBeAg阳性2 081例,HBeAg阴性4 868例,中位随访时间为8年,多因素Cox回归分析表明,HBeAg阳性患者中,基线HBV DNA为6~7 log10 IU/mL患者的HCC风险最高(调整的HR为4.98,P<0.001),HBV DNA>8 log10 IU/mL患者最低(调整的HR为0.90)。分析各年龄组患者结果表明,HBV DNA为6~7 log10 IU/mL和4~6 log10 IU/mL的患者发生HCC风险高于HBV DNA>8 log10 IU/mL患者;HBeAg阴性患者中,HBV DNA>5 log10 IU/mL和4~5 log10 IU/mL患者发生HCC风险高于HBV DNA<3 log10 IU/mL患者,表明HBeAg阳性和阴性HBV感染期(既往分别称免疫耐受期和免疫控制期)的不确定期患者发生HCC风险较高(P<0.001)(图2)。
美国、新加坡和中国台湾地区联合研究[11]报道,对1 303例基线为不确定期和1 370非活动期慢性HBV感染者随访10年,前者的HCC累积发生率(2.7%)较后者(0.6%)高至4.5倍。其中686例随访10年仍为不确定期患者的HCC累积发生率为4.6%;857例在随访10年仍为非活动期患者的HCC累积发生率为0.5%,前者较后者高至9.2倍。多变量分析表明,随访10年维持在不确定期、年龄≥40岁和≥45岁慢性乙型肝炎患者累计发生HCC风险,较年龄<40岁和<45岁患者分别高9.06倍和18.40倍。因此,对40岁及以上不确定期慢性乙型肝炎患者更应考虑抗病毒治疗。
4. 对不确定期患者抗病毒治疗可显著降低HCC发病率
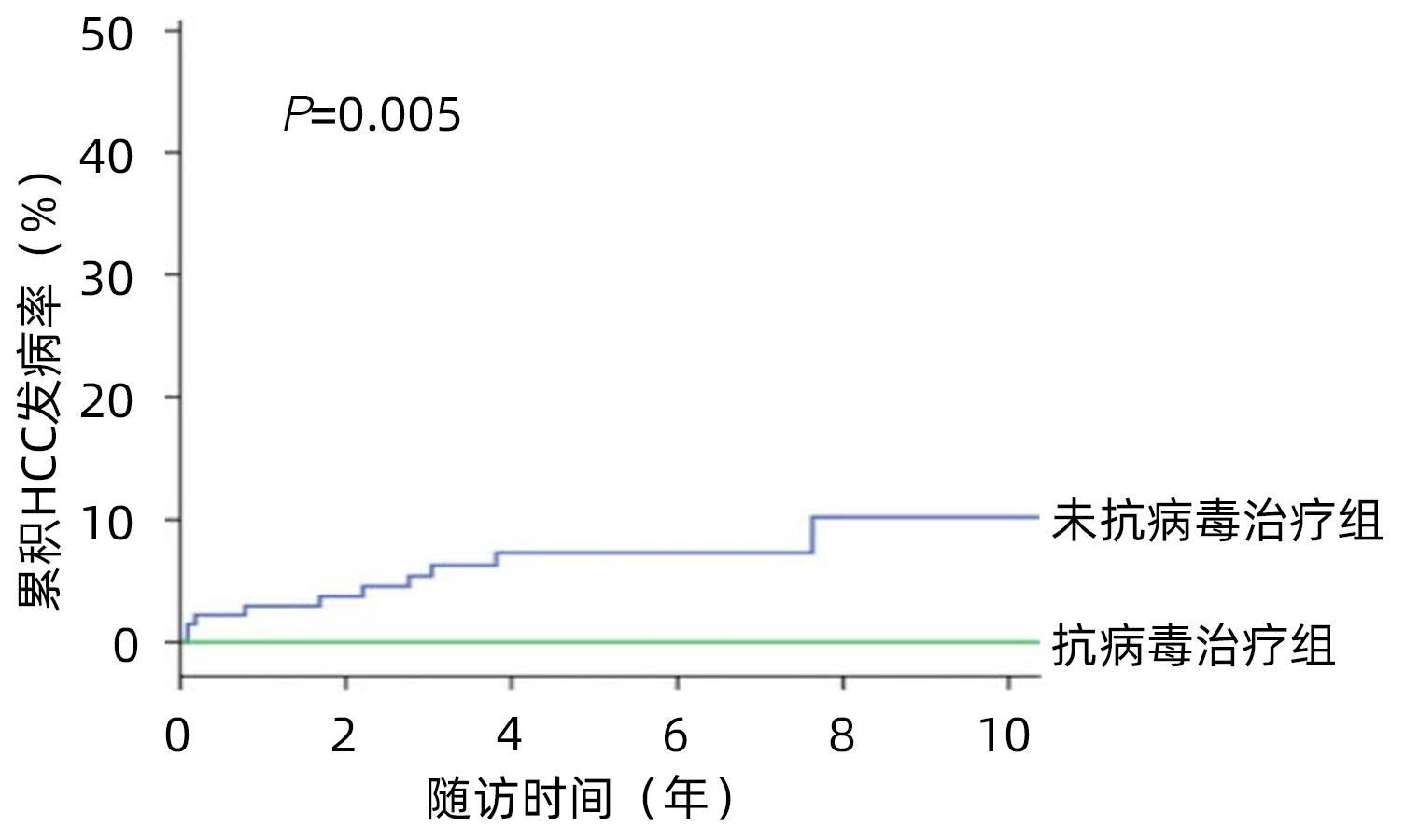
Teng等[19]应用3 527例慢性HBV感染者的REVEAL-HBV队列,建立了预测HCC的评分系统,并对按2015年版亚太肝病学会乙型肝炎管理临床实践指南[20]定为不确定期(ALT<80 U/L或HBV DNA<2 000 IU/mL)的749例患者进行了分析,其中135例为HCC高风险(计分≥8),按模型推算,在高风险组中,接受抗病毒治疗患者的HCC年发病率为0,未接受抗病毒治疗患者为1.96%,两者有显著差异(P=0.005)(图3)。最近,Huang等[21]报道美国、欧洲和亚洲14个中心的研究结果,接受抗病毒治疗的不确定期患者10年HCC累积发生率为4%,显著低于未治疗组(15%)。
5. 小结
不确定期慢性HBV感染者的肝脏有显著坏死炎症和纤维化的比例较高,发生HBV相关的HCC风险较高,抗病毒治疗可显著降低HCC发病率。
-
表 1 慢性HBV感染者中不确定期患者的比例
Table 1. The proportion of individuals in the indeterminate phase among patients with chronic HBV infection
作者 总例数 不确定期例数 比例(%) 诊断标准 Yao等(2021)[9] 4 759 1 323 27.8 AASLD(2018) Duan等(2021)[10] 327 122 37.3 CSH/CSID(2019) Huang等(2022)[11] 3 366 1 303 38.7 AASLD(2018) Jiang等(2023)[12] 634 377 59.5 CSH/CSID(2019) Wang等(2023)[13] 1 043 242 23.2 AASLD(2018) Xu等(2023)[14] 3 462 1 444 41.7 CSH/CSID(2022) Ju等(2023)[15] 1 544 574 37.2 AASLD(2018) 注:AASLD,美国肝病学会;CSH,中华医学会肝病学分会;CSID,中华医学会感染病学分会。 表 2 HBeAg阳性和阴性慢性HBV感染期的不确定期患者肝组织病理学
Table 2. Liver histopathology of indeterminate-phase patients with HBeAg-positive and HBeAg-negative chronic HBV infection
作者 显著坏死炎症 显著纤维化 显著组织学病变 Liu等(2022)[16] 68.3%(397/581) 58.5%(340/581) 49.7%(289/581) Jiang等(2023)[12] 29.2%(110/377) 34.0%(128/377) 40.6%(153/377) Wang等(2023)[13] HBeAg阳性 84.4%(38/45) 73.3%(33/45) 91.1%(41/45) HBeAg阴性 54.3%(107/197) 53.3%(105/197) 68.5%(135/197) 小计 59.9%(145/242) 57.0%(138/242) 72.7%(176/242) -
[1] Chinese Society of Hepatology, Chinese Medical Association. Experts opinon on expanding anti-HBV treatment for chronic hepatitis B[J]. Chin J Hepatol, 2022, 30( 2): 131- 136. DOI: 10.3760/cma.j.cn501113-20220209-00060.中华医学会肝病学分会. 扩大慢性乙型肝炎抗病毒治疗的专家意见[J]. 中华肝脏病杂志, 2022, 30( 2): 131- 136. DOI: 10.3760/cma.j.cn501113-20220209-00060. [2] Chinese Society of Hepatology, Chinese Medical Association; Chinese Society of Infectious Diseases, Chinese Medical Association. Guidelines for the prevention and treatment of chronic hepatitis B(version 2022)[J]. Chin J Hepatol, 2022, 30( 12): 1309- 1331. DOI: 10.3760/cma.j.cn501113-20221204-00607.中华医学会肝病学分会, 中华医学会感染病学分会. 慢性乙型肝炎防治指南(2022年版)[J]. 中华肝脏病杂志, 2022, 30( 12): 1309- 1331. DOI: 10.3760/cma.j.cn501113-20221204-00607. [3] KUMAR M, SARIN SK, HISSAR S, et al. Virologic and histologic features of chronic hepatitis B virus-infected asymptomatic patients with persistently normal ALT[J]. Gastroenterology, 2008, 134( 5): 1376- 1384. DOI: 10.1053/j.gastro.2008.02.075. [4] HSU YN, PAN CQ, ABBASI A, et al. Clinical presentation and disease phases of chronic hepatitis B using conventional versus modified ALT criteria in Asian Americans[J]. Dig Dis Sci, 2014, 59( 4): 865- 871. DOI: 10.1007/s10620-014-3054-1. [5] European Association for the Study of the Liver. EASL 2017 Clinical Practice Guidelines on the management of hepatitis B virus infection[J]. J Hepatol, 2017, 67( 2): 370- 398. DOI: 10.1016/j.jhep.2017.03.021. [6] MARTIN P, NGUYEN MH, DIETERICH DT, et al. Treatment algorithm for managing chronic hepatitis B virus infection in the United States: 2021 update[J]. Clin Gastroenterol Hepatol, 2022, 20( 8): 1766- 1775. DOI: 10.1016/j.cgh.2021.07.036. [7] CHOI HSJ, TONTHAT A, JANSSEN HLA, et al. Aiming for functional cure with established and novel therapies for chronic hepatitis B[J]. Hepatol Commun, 2022, 6( 5): 935- 949. DOI: 10.1002/hep4.1875. [8] DUSHEIKO G, AGARWAL K, MAINI MK. New approaches to chronic hepatitis B[J]. N Engl J Med, 2023, 388( 1): 55- 69. DOI: 10.1056/NEJMra2211764. [9] YAO KF, LIU JC, WANG J, et al. Distribution and clinical characteristics of patients with chronic hepatitis B virus infection in the grey zone[J]. J Viral Hepat, 2021, 28( 7): 1025- 1033. DOI: 10.1111/jvh.13511. [10] DUAN MH, CHI XL, XIAO HM, et al. High-normal alanine aminotransferase is an indicator for liver histopathology in HBeAg-negative chronic hepatitis B[J]. Hepatol Int, 2021, 15( 2): 318- 327. DOI: 10.1007/s12072-021-10153-2. [11] HUANG DQ, LI XH, LE MH, et al. Natural history and hepatocellular carcinoma risk in untreated chronic hepatitis B patients with indeterminate phase[J]. Clin Gastroenterol Hepatol, 2022, 20( 8): 1803- 1812.e 5. DOI: 10.1016/j.cgh.2021.01.019. [12] JIANG SW, LIAN X, HU AR, et al. Liver histopathological lesions is severe in patients with normal alanine transaminase and low to moderate hepatitis B virus DNA replication[J]. World J Gastroenterol, 2023, 29( 16): 2479- 2494. DOI: 10.3748/wjg.v29.i16.2479. [13] WANG J, YAN XM, ZHU L, et al. Significant histological disease of patients with chronic hepatitis B virus infection in the grey zone[J]. Aliment Pharmacol Ther, 2023, 57( 5): 464- 474. DOI: 10.1111/apt.17272. [14] XU XQ, WANG H, SHAN S, et al. The impact of the definitions of clinical phases on the profiles of grey-zone patients with chronic hepatitis B virus infection[J]. Viruses, 2023, 15( 5): 1212. DOI: 10.3390/v15051212. [15] JU YH, HAN GR, ZHANG P, et al. Staging and clinical characteristics of pregnant women with chronic hepatitis B virus infection: A retrospective cohort study from Nanjing, China[J]. J Obstet Gynaecol Res, 2023, 49( 10): 2427- 2435. DOI: 10.1111/jog.15753. [16] LIU JC, WANG J, YAN XM, et al. Presence of liver inflammation in Asian patients with chronic hepatitis B with normal ALT and detectable HBV DNA in absence of liver fibrosis[J]. Hepatol Commun, 2022, 6( 4): 855- 866. DOI: 10.1002/hep4.1859. [17] CHOI GH, KIM GA, CHOI J, et al. High risk of clinical events in untreated HBeAg-negative chronic hepatitis B patients with high viral load and no significant ALT elevation[J]. Aliment Pharmacol Ther, 2019, 50( 2): 215- 226. DOI: 10.1111/apt.15311. [18] KIM GA, HAN S, CHOI GH, et al. Moderate levels of serum hepatitis B virus DNA are associated with the highest risk of hepatocellular carcinoma in chronic hepatitis B patients[J]. Aliment Pharmacol Ther, 2020, 51( 11): 1169- 1179. DOI: 10.1111/apt.15725. [19] TENG W, CHANG TT, YANG HI, et al. Risk scores to predict HCC and the benefits of antiviral therapy for CHB patients in gray zone of treatment guidelines[J]. Hepatol Int, 2021, 15( 6): 1421- 1430. DOI: 10.1007/s12072-021-10263-x. [20] SARIN SK, KUMAR M, LAU GK, et al. Asian-Pacific clinical practice guidelines on the management of hepatitis B: A 2015 update[J]. Hepatol Int, 2016, 10( 1): 1- 98. DOI: 10.1007/s12072-015-9675-4. [21] HUANG DQ, TRAN A, YEH ML, et al. Antiviral therapy substantially reduces HCC risk in patients with chronic hepatitis B infection in the indeterminate phase[J]. Hepatology, 2023, 78( 5): 1558- 1568. DOI: 10.1097/HEP.0000000000000459. 期刊类型引用(5)
1. 艾骞,赵智蓉,吴月,李海雯,李生浩,杨永锐. 不确定期慢性乙型肝炎病毒感染患者抗病毒疗效及安全性分析. 昆明医科大学学报. 2025(01): 51-59 .  百度学术
百度学术2. 丁洋,窦晓光. 早筛早诊早治,阻止乙型肝炎病毒感染相关不良临床结局. 中国实用内科杂志. 2025(02): 89-91+95 .  百度学术
百度学术3. 王福生,朱世殊,张敏,王建设,李双杰,福军亮,李元元,郭玉明,李静,许红梅,欧阳文献,南月敏,舒赛男,党双锁,徐小元,李太生,侯金林. 儿童慢性乙型肝炎防治专家共识. 传染病信息. 2024(02): 97-112 .  百度学术
百度学术4. 中华医学会感染病学分会,中华医学会肝病学分会,中华医学会儿科学分会感染学组,国家感染性疾病临床医学研究中心. 儿童慢性乙型肝炎防治专家共识. 中华肝脏病杂志. 2024(05): 435-448 .  百度学术
百度学术5. 中华医学会肝病学分会肝炎学组,中华肝脏病杂志编辑委员会. 加速消除乙型肝炎病毒感染:扩大预防和治疗专家建议. 中华肝脏病杂志. 2024(06): 497-503 .  百度学术
百度学术其他类型引用(1)
-




 PDF下载 ( 761 KB)
PDF下载 ( 761 KB)

 下载:
下载:




 下载:
下载:


 百度学术
百度学术