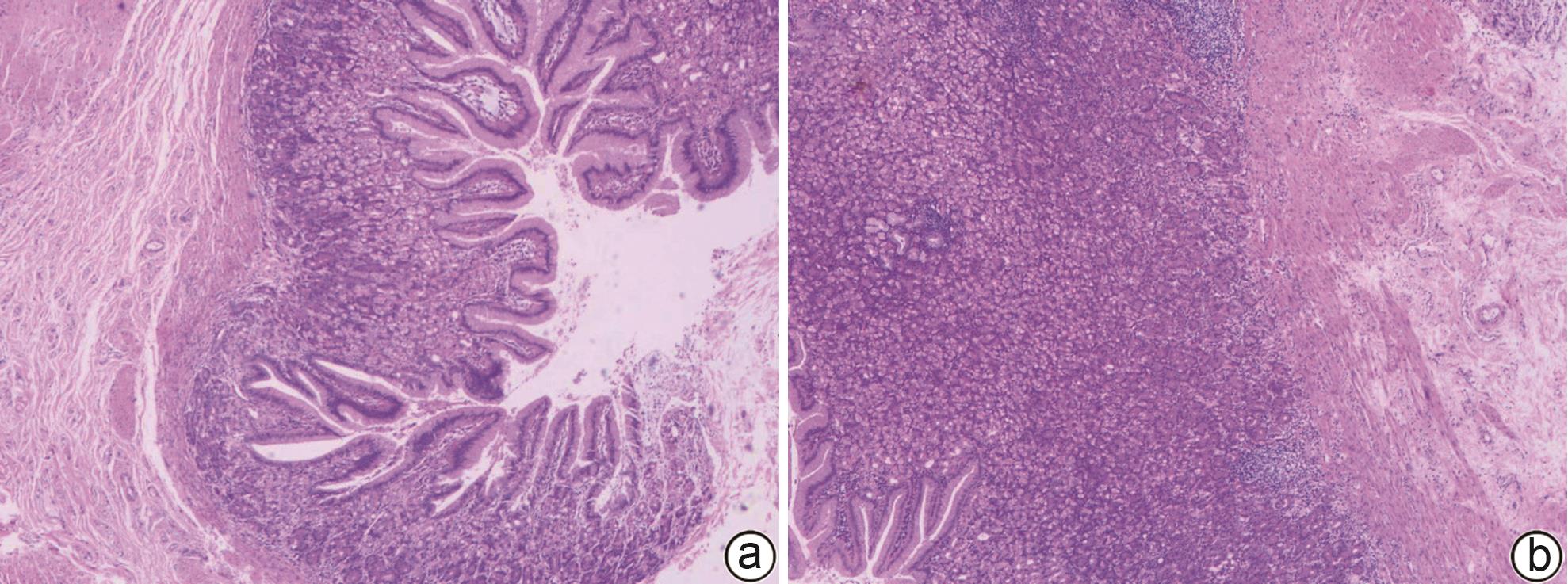
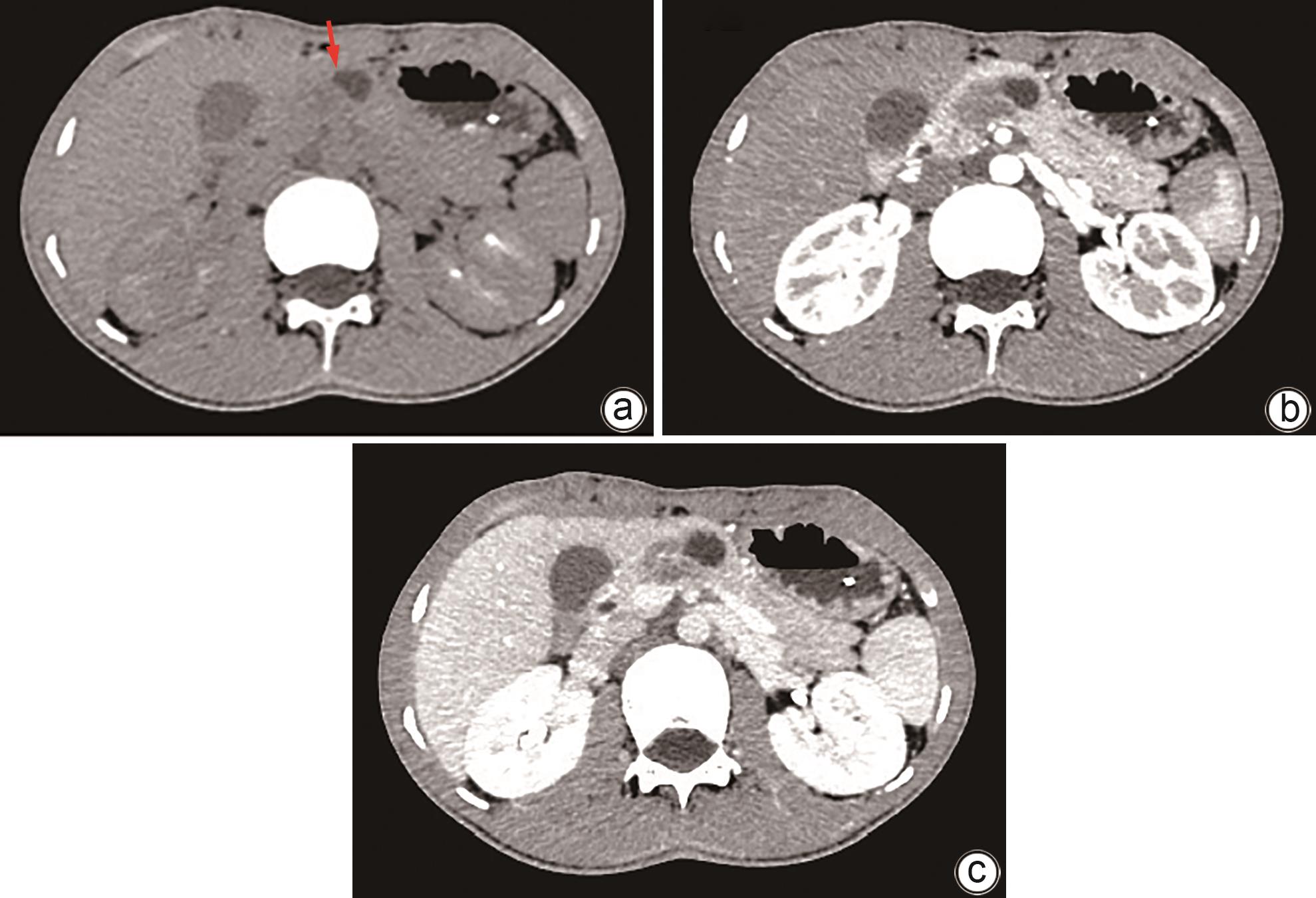
胰腺错构瘤1例报告
DOI: 10.12449/JCH241024
伦理学声明:本例报告已获得患者知情同意。
利益冲突声明:本文不存在任何利益冲突。
作者贡献声明:冯泉凯负责文献复习、收集数据、资料分析、撰写论文;李捷负责病例诊断、指导写作、修改论文并最后定稿。
-
摘要: 胰腺错构瘤是一种罕见的胰腺良性病变,缺乏典型的临床症状和影像学特征,术前难以诊断。常由于无法排除恶性肿瘤的风险而行外科手术治疗,从而造成正常胰腺组织的损伤。此外,胰腺错构瘤中出现胃黏膜组织尚未有报道,本文同时回顾了国内外有关胰腺错构瘤的文献,总结其临床表现及影像学特点,有助于术前诊断。Abstract: Pancreatic hamartoma is a rare benign lesion of the pancreas characterized by a lack of typical clinical symptoms and imaging features, which leads to the difficulty in diagnosis before surgery. Since surgical intervention is often performed due to the inability to exclude the risk of malignant tumor, it may cause damage to normal pancreatic tissue. In addition, the presence of gastric mucosal tissue in pancreatic hamartoma has not been reported in the literature. This article reviews the articles on pancreatic hamartoma in China and globally and summarizes its clinical and imaging features, so as to provide help for preoperative diagnosis.
-
Key words:
- Pancreatic Neoplasms /
- Hamartoma /
- Diagnosis, Differential
-
-
[1] NAGATA S, YAMAGUCHI K, INOUE T, et al. Solid pancreatic hamartoma[J]. Pathol Int, 2007, 57( 5): 276- 280. DOI: 10.1111/j.1440-1827.2007.02090.x. [2] HEALD B, BURKE CA, KALADY M, et al. ACG guidelines on management of PTEN-hamartoma tumor syndrome: Does the evidence support so much so young?[J]. Am J Gastroenterol, 2015, 110( 12): 1733- 1734. DOI: 10.1038/ajg.2015.368. [3] MATSUSHITA D, KURAHARA H, MATAKI Y, et al. Pancreatic hamartoma: A case report and literature review[J]. BMC Gastroenterol, 2016, 16: 3. DOI: 10.1186/s12876-016-0419-2. [4] ANTHONY PP, FABER RG, RUSSELL RC. Pseudotumours of the pancreas[J]. Br Med J, 1977, 1( 6064): 814. DOI: 10.1136/bmj.1.6064.814. [5] MURAKAMI T, YAMAZAKI M, YAMAZAKI K, et al. A distinctive myoepithelial hamartoma of the pancreas histologically confirmed in the mother of a previously reported patient[J]. Pancreatology, 2016, 16( 3): 464- 468. DOI: 10.1016/j.pan.2015.12.178. [6] DELGADO PI, CORREA-MEDINA M, ROJAS CP. Pancreatic hamartoma in a premature Trisomy 18 female[J]. Autops Case Rep, 2017, 7( 4): 26- 29. DOI: 10.4322/acr.2017.041. [7] ADDEO P, TUDOR G, OUSSOULTZOGLOU E, et al. Pancreatic hamartoma[J]. Surgery, 2014, 156( 5): 1284- 1285. DOI: 10.1016/j.surg.2013.02.021. [8] NAHM CB, NAJDAWI F, REAGH J, et al. Pancreatic hamartoma: A sheep in wolf’s clothing[J]. ANZ J Surg, 2019, 89( 6): E265- E267. DOI: 10.1111/ans.14332. [9] ZHANG JW, WANG H, TANG XL, et al. Pancreatic hamartoma, a rare benign disease of the pancreas: A case report[J]. Oncol Lett, 2016, 11( 6): 3925- 3928. DOI: 10.3892/ol.2016.4535. [10] ZHOU B, LI GG, XU SY, et al. Pancreatic lipomatous hamartoma mimicking other pancreatic tumor: A case report and literature review[J]. Am J Transl Res, 2020, 12( 10): 6682- 6688. [11] INOUE H, TAMEDA M, YAMADA R, et al. Pancreatic hamartoma: A rare cause of obstructive jaundice[J]. Endoscopy, 2014, 46(Suppl 1 UCTN): E157- E158. DOI: 10.1055/s-0034-1364953. [12] YAMAGUCHI H, AISHIMA S, ODA Y, et al. Distinctive histopathologic findings of pancreatic hamartomas suggesting their“hamartomatous” nature: A study of 9 cases[J]. Am J Surg Pathol, 2013, 37( 7): 1006- 1013. DOI: 10.1097/PAS.0b013e318283ce4c. [13] PAUSER U, KOSMAHL M, KRUSLIN B, et al. Pancreatic solid and cystic hamartoma in adults: Characterization of a new tumorous lesion[J]. Am J Surg Pathol, 2005, 29( 6): 797- 800. DOI: 10.1097/01.pas.0000157748.18591.d7. [14] AHN AR, SONG JS, YANG JD, et al. Pancreatic hamartoma mimicking neuroendocrine tumor[J]. Pathol Int, 2021, 71( 11): 789- 791. DOI: 10.1111/pin.13153. [15] KATAYAMA H, AZUMA K, KONERI K, et al. A typical case of resected pancreatic hamartoma: A case report and literature review on imaging and pathology[J]. Surg Case Rep, 2020, 6( 1): 107. DOI: 10.1186/s40792-020-00869-y. [16] BRAVO-TAXA M, BERROSPI-ESPINOZA F, TAXA-ROJAS L. Pancreatic lipomatous hamartoma: A case report and literature review[J]. Rev Gastroenterol Peru, 2023, 43( 2): 161- 165. [17] TANAKA M, USHIKU T, IKEMURA M, et al. Pancreatic lipomatous hamartoma: A hitherto unrecognized variant[J]. Am J Surg Pathol, 2018, 42( 7): 891- 897. DOI: 10.1097/PAS.0000000000001075. [18] NAGANO H, NAKAJO M, FUKUKURA Y, et al. A small pancreatic hamartoma with an obstruction of the main pancreatic duct and avid FDG uptake mimicking a malignant pancreatic tumor: A systematic case review[J]. BMC Gastroenterol, 2017, 17( 1): 146. DOI: 10.1186/s12876-017-0704-8. [19] HAN YE, PARK BJ, SUNG DJ, et al. Computed tomography and magnetic resonance imaging findings of pancreatic hamartoma: A case report and literature review[J]. Clin Imaging, 2018, 52: 32- 35. DOI: 10.1016/j.clinimag.2018.06.002. [20] CUI H, LIAN YQ, CHEN F. Imaging findings for pancreatic Hamartoma: Two case reports and a review of the literature[J]. BMC Gastroenterol, 2020, 20( 1): 37. DOI: 10.1186/s12876-020-1185-8. [21] TOYAMA K, MATSUSAKA Y, OKUDA S, et al. A case of pancreatic hamartoma with characteristic radiological findings: Radiological-pathological correlation[J]. Abdom Radiol, 2020, 45( 7): 2244- 2248. DOI: 10.1007/s00261-020-02425-6. [22] NOGUCHI T, RYOZAWA S, MIZUIDE M, et al. Pancreatic hamartoma difficult to diagnose preoperatively[J]. Intern Med, 2021, 60( 13): 2055- 2059. DOI: 10.2169/internalmedicine.5982-20. -



 PDF下载 ( 1146 KB)
PDF下载 ( 1146 KB)

 下载:
下载: