肝硬化门脉性肺动脉高压危险因素分析及预测模型构建
DOI: 10.12449/JCH240914
Risk factors for portopulmonary hypertension in liver cirrhosis and construction of a predictive model
-
摘要:
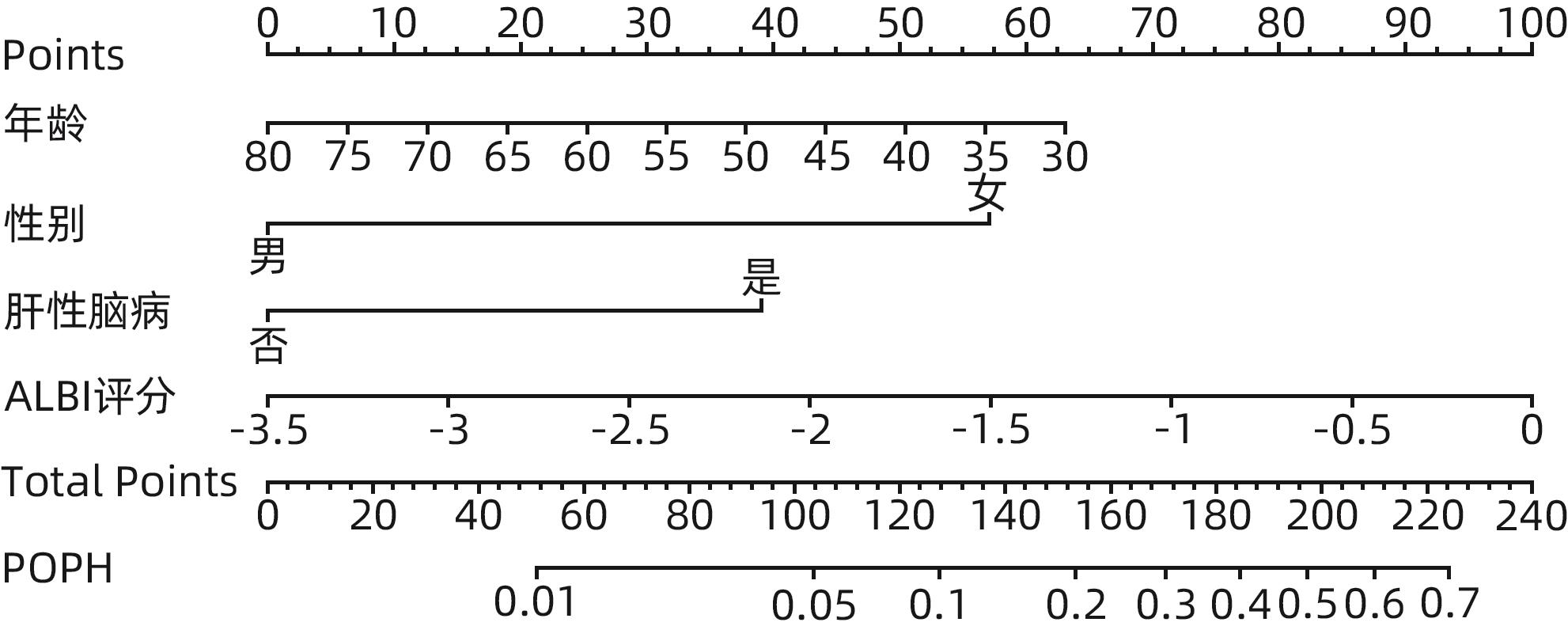
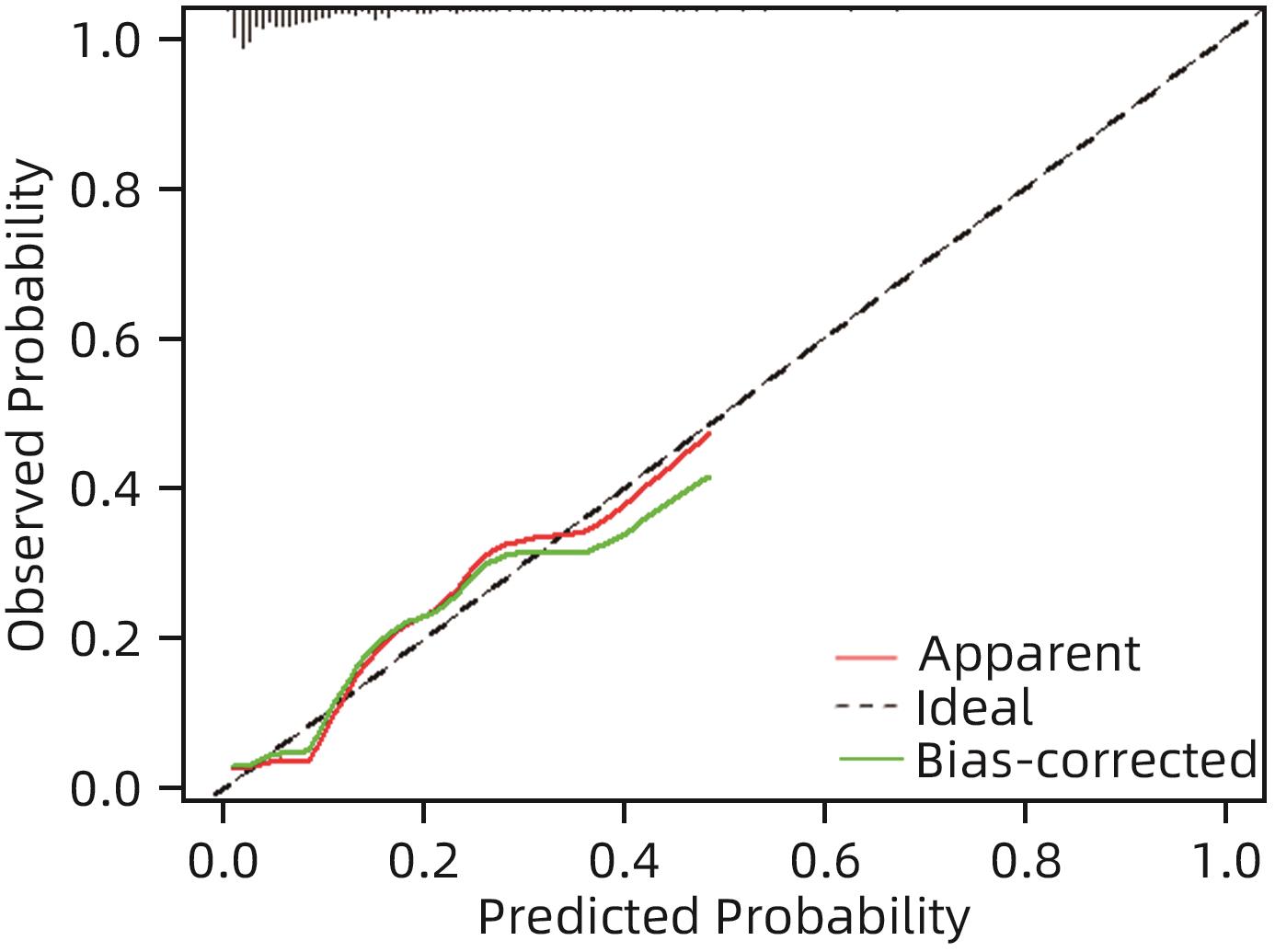
目的 探索肝硬化门脉性肺动脉高压(POPH)的危险因素,构建无创化预测模型。 方法 回顾性分析2013年1月—2022年8月在河北医科大学第三医院住院的310例肝硬化门静脉高压患者的临床资料,依据超声估测的肺动脉收缩压是否≥40 mmHg分为POPH组(n=31)和非POPH组(n=279)。符合正态分布的计量资料2组间比较采用成组t检验,不符合正态分布的计量资料2组间比较采用Mann-Whitney U检验;计数资料2组间比较采用χ2检验或Fisher确切概率法。应用二元Logistic回归分析筛选独立危险因素,并构建列线图预测模型,采用Bootstrap重抽样法进行内部验证,用C指数和校准曲线评价模型区分度和一致性。用rms包绘制列线图。 结果 与非POPH组相比,POPH组平均年龄偏小,女性、肝性脑病、Child-Pugh C级占比较高,DBil、MELD评分、ALBI评分、国际标准化比值、凝血酶原时间、FIB-4指数、LOK评分、Forns指数较高,但Alb、ALT、GGT、血红蛋白、总胆固醇、甘油三酯水平较低,差异均具有统计学意义(P值均<0.05)。多因素分析结果显示,性别(OR=0.172,95%CI:0.064~0.462,P<0.001)、年龄(OR=0.944,95%CI:0.901~0.989,P=0.016)、ALBI评分(OR=3.091,95%CI:1.100~8.687,P=0.032)和肝性脑病(OR=3.466,95%CI:1.331~9.031,P=0.011)是POPH的独立影响因素。基于以上危险因素建立的肝硬化POPH预测模型的C指数为0.796(95%CI:0.701~0.890),提示模型区分度良好,校准曲线显示模型校准能力较好,提示模型具有一定预测效能。 结论 年轻女性、ALBI评分升高、合并肝性脑病是肝硬化患者发生POPH的独立危险因素,基于上述因素建立的预测模型具有一定的临床应用价值。 Abstract:Objective To investigate the risk factors for portopulmonary hypertension (POPH) in liver cirrhosis, and to construct a noninvasive predictive model. Methods A retrospective analysis was performed for the clinical data of 310 cirrhotic patients with portal hypertension who were hospitalized in The Third Affiliated Hospital of Hebei Medical University from January 2013 to August 2022, and according to whether pulmonary artery systolic pressure was ≥40 mmHg on ultrasound, the patients were divided into POPH group with 31 patients and non-POPH group with 279 patients. The independent-samples t test was used for comparison of normally distributed continuous data between two groups, and the Mann-Whitney U test was used for comparison of non-normally distributed continuous data between two groups; the chi-square test or the Fisher’s exact test was used for comparison of categorical data between two groups. A binary Logistic regression analysis was used to determine the independent risk factors for POPH, and a nomogram prediction model was constructed. The Bootstrap resampling method was used for internal validation, and C-index and calibration curve were used to assess the discriminatory ability and consistency of the model. The rms package was used to plot the nomogram. Results Compared with the non-POPH group, the POPH group had a significantly younger age, a significantly higher proportion of women or patients with hepatic encephalopathy or Child-Pugh class C disease, and significantly higher levels of direct bilirubin, Model for End-Stage Liver Disease score, albumin-bilirubin (ALBI) score, international normalized ratio, prothrombin time, FIB-4 index, LOK score, and Forns index, as well as significantly lower levels of serum albumin, alanine aminotransferase, gamma-glutamyl transpeptidase, hemoglobin, total cholesterol, and triglycerides (all P<0.05). The multivariate analysis showed that sex (odds ratio [OR]=0.172, 95% confidence interval [CI]: 0.064 — 0.462, P<0.001), age (OR=0.944, 95%CI: 0.901 — 0.989, P=0.016), ALBI score (OR=3.091, 95%CI: 1.100 — 8.687, P=0.032), and hepatic encephalopathy (OR=3.466, 95%CI: 1.331 — 9.031, P=0.011) were independent risk factors for POPH. A predictive model for POPH in liver cirrhosis was established based on the above independent risk factors, with a C-index of 0.796 (95%CI: 0.701 — 0.890), suggesting that the model had good discriminatory ability, and the calibration curve showed that the model had good calibration ability, suggesting that the model had certain predictive efficacy. Conclusion Young female individuals, elevated ALBI score, and comorbidity with hepatic encephalopathy are independent risk factors for POPH in patients with liver cirrhosis, and the predictive model established based on these factors has a certain clinical application value. -
Key words:
- Liver Cirrhosis /
- Hypertension, Portal /
- Pulmonary Arterial Hypertension /
- Risk Factors /
- Nomograms
-
表 1 肝硬化POPH组和非POPH组基线特征
Table 1. Baseline characteristics of POPH and non-POPH in liver cirrhosis
指标 POPH组(n=31) 非POPH组(n=279) 统计值 P值 性别[例(%)] χ2=12.03 0.001 男 11(35.48) 187(67.03) 女 20(64.52) 92(32.97) 年龄(岁) 52.39±13.00 56.14±9.41 t=2.02 0.044 Alb(g/L) 30.79(26.63~35.78) 33.90(29.46~38.06) U=3 004.00 0.005 ALT(U/L) 23.00(18.00~32.00) 30.00(18.00~46.00) U=3 261.00 0.025 DBil(μmol/L) 22.00(10.32~72.08) 14.36(7.72~32.34) U=3 137.00 0.012 ALP(U/L) 100.00(69.00~152.00) 99.00(71.00~142.00) U=4 224.00 0.832 GGT(U/L) 27.00(16.00~44.00) 39.00(24.00~89.00) U=3 210.00 0.019 肌酸激酶(U/L) 64.60(43.00~84.80) 70.60(43.70~112.60) U=4 031.00 0.535 乳酸脱氢酶(U/L) 219.25(188.00~261.91) 200.00(160.44~248.24) U=3 612.50 0.133 总胆固醇(mmol/L) 2.64(1.72~3.23) 3.24(2.60~3.92) U=2 816.50 0.001 甘油三酯(mmol/L) 0.63(0.51~1.13) 0.83(0.64~1.08) U=3 360.50 0.042 白细胞计数(×109/L) 3.21(2.21~4.46) 3.47(2.46~4.93) U=3 993.50 0.484 中性粒细胞百分比(%) 63.10(57.10~71.20) 62.53(55.20~72.10) U=4 047.00 0.558 血红蛋白(g/L) 90.43±25.90 107.62±27.47 t=3.49 0.001 血小板计数(×109/L) 46.70(26.00~84.30) 61.00(41.00~92.30) U=3 538.50 0.097 国际标准化比值 1.65(1.24~1.84) 1.29(1.14~1.53) U=2 642.50 <0.001 凝血酶原时间(g/L) 17.90(13.70~20.60) 14.50(12.70~17.20) U=2 769.50 0.001 纤维蛋白原(g/L) 1.65(1.06~2.25) 1.84(1.44~2.33) U=3 572.50 0.112 D-二聚体(mg/L) 1.20(0.60~2.20) 0.80(0.20~2.02) U=3 415.50 0.054 MELD评分 17.00(9.00~21.00) 12.00(9.00~16.00) U=3 315.50 0.033 ALBI评分 -1.45(-1.90~0.97) -1.79(-2.30~1.36) U=2 835.00 0.002 APRI 2.06(1.07~3.44) 1.68(0.94~2.92) U=3 878.50 0.346 FIB-4指数 10.32(5.04~17.49) 6.68(3.97~10.31) U=3 097.00 0.010 S指数 0.68(0.44~1.06) 0.62(0.30~1.46) U=4 157.00 0.723 LOK评分 4.77(2.93~6.52) 2.49(1.32~4.34) U=2 671.00 <0.001 Forns指数 12.41±1.91 11.61±1.99 t=-2.21 0.033 肝病病因[例(%)] χ2=14.06 0.061 乙型肝炎 9(29.03) 157(56.27) 丙型肝炎 3(9.68) 18(6.45) 酒精性肝病 5(16.13) 33(11.83) 自身免疫性肝病 4(12.90) 16(5.73) 药物性肝炎 2(6.45) 5(1.79) 隐源性肝硬化 8(25.81) 44(15.77) 肝豆状核变性 0(0.00) 4(1.43) 非酒精性脂肪性肝病 0(0.00) 2(0.72) Child-Pugh分级[例(%)] χ2=6.72 0.010 B级 12(38.71) 175(62.72) C级 19(61.29) 104(37.28) 肝性脑病[例(%)] χ2=10.05 0.002 有 14(45.16) 56(20.07) 无 17(54.84) 223(79.93) 表 2 肝硬化POPH独立影响因素
Table 2. Multivariable analysis of POPH in liver cirrhosis
指标 B值 Wald OR 95%CI P值 性别(男) -1.761 0.504 0.172 0.064~0.462 <0.001 年龄 -0.058 0.024 0.944 0.901~0.989 0.016 ALBI评分 1.128 0.527 3.091 1.100~8.687 0.032 肝性脑病(是) 1.243 0.489 3.466 1.331~9.031 0.011 常量 3.273 2.603 26.402 0.209 注:性别赋值,女=0,男=1;肝性脑病赋值,否=0,是=1。
-
[1] KHADERI S, KHAN R, SAFDAR Z, et al. Long-term follow-up of portopulmonary hypertension patients after liver transplantation[J]. Liver Transpl, 2014, 20( 6): 724- 727. DOI: 10.1002/lt.23870. [2] GBD Cirrhosis Collaborators. The global, regional, and national burden of cirrhosis by cause in 195 countries and territories, 1990-2017: A systematic analysis for the Global Burden of Disease Study 2017[J]. Lancet Gastroenterol Hepatol, 2020, 5( 3): 245- 266. DOI: 10.1016/S2468-1253(19)30349-8. [3] JOSE A, SHAH SA, ANWAR N, et al. Pulmonary vascular resistance predicts mortality and graft failure in transplantation patients with portopulmonary hypertension[J]. Liver Transpl, 2021, 27( 12): 1811- 1823. DOI: 10.1002/lt.26091. [4] Chinese Society of Hepatology, Chinese Medical Association. Chinese guidelines on the management of liver cirrhosis[J]. J Clin Hepatol, 2019, 35( 11): 2408- 2425. DOI: 10.3969/j.issn.1001-5256.2019.11.006.中华医学会肝病学分会. 肝硬化诊治指南[J]. 临床肝胆病杂志, 2019, 35( 11): 2408- 2425. DOI: 10.3969/j.issn.1001-5256.2019.11.006. [5] MCLAUGHLIN VV, ARCHER SL, BADESCH DB, et al. ACCF/AHA 2009 expert consensus document on pulmonary hypertension a report of the American College of Cardiology Foundation Task Force on Expert Consensus Documents and the American Heart Association developed in collaboration with the American College of Chest Physicians; American Thoracic Society, Inc.; and the Pulmonary Hypertension Association[J]. J Am Coll Cardiol, 2009, 53( 17): 1573- 1619. DOI: 10.1016/j.jacc.2009.01.004. [6] TU Y, LI X, CHEN MJ, et al. Value of platelet count and related scoring models in predicting the prognosis of hepatitis B virus-related acute-on-chronic liver failure[J]. J Clin Hepatol, 2023, 39( 6): 1308- 1312. DOI: 10.3969/j.issn.1001-5256.2023.06.009.涂颖, 李雪, 陈美娟, 等. 血小板计数及相关评分模型对HBV相关慢加急性肝衰竭预后的预测价值[J]. 临床肝胆病杂志, 2023, 39( 6): 1308- 1312. DOI: 10.3969/j.issn.1001-5256.2023.06.009. [7] WANG L, FENG YM, MA XW, et al. Diagnostic efficacy of noninvasive liver fibrosis indexes in predicting portal hypertension in patients with cirrhosis[J]. PLoS One, 2017, 12( 8): e0182969. DOI: 10.1371/journal.pone.0182969. [8] MA LJ, HE C. The relationship between APRI and S index and Child Pugh in patients with hepatitis B cirrhosis[J]. Chin Hepatol, 2019, 24( 4): 448- 449. DOI: 10.3969/j.issn.1008-1704.2019.04.032.马丽君, 何聪. APRI及S指数与乙型肝炎肝硬化Child-Pugh肝功能分级的关系[J]. 肝脏, 2019, 24( 4): 448- 449. DOI: 10.3969/j.issn.1008-1704.2019.04.032. [9] KAWUT SM, KROWKA MJ, TROTTER JF, et al. Clinical risk factors for portopulmonary hypertension[J]. Hepatology, 2008, 48( 1): 196- 203. DOI: 10.1002/hep.22275. [10] CASTAÑO G, SOOKOIAN S. Female sex and autoimmune hepatitis and the risk of portopulmonary hypertension[J]. Hepatology, 2008, 48( 6): 2090. DOI: 10.1002/hep.22599. [11] DUBROCK HM, CARTIN-CEBA R, CHANNICK RN, et al. Sex differences in portopulmonary hypertension[J]. Chest, 2021, 159( 1): 328- 336. DOI: 10.1016/j.chest.2020.07.081. [12] ROBERTS KE, FALLON MB, KROWKA MJ, et al. Genetic risk factors for portopulmonary hypertension in patients with advanced liver disease[J]. Am J Respir Crit Care Med, 2009, 179( 9): 835- 842. DOI: 10.1164/rccm.200809-1472OC. [13] AL-NAAMANI N, KROWKA MJ, FORDE KA, et al. Estrogen signaling and portopulmonary hypertension: The pulmonary vascular complications of liver disease study(PVCLD2)[J]. Hepatology, 2021, 73( 2): 726- 737. DOI: 10.1002/hep.31314. [14] SHAO YM, YIN X, QIN TT, et al. Prevalence and associated factors of portopulmonary hypertension in patients with portal hypertension: A case-control study[J]. Biomed Res Int, 2021, 2021: 5595614. DOI: 10.1155/2021/5595614. [15] KAWAGUCHI T, HONDA A, SUGIYAMA Y, et al. Association between the albumin-bilirubin(ALBI) score and severity of portopulmonary hypertension(PoPH): A data-mining analysis[J]. Hepatol Res, 2021, 51( 12): 1207- 1218. DOI: 10.1111/hepr.13714. [16] JOHNSON PJ, BERHANE S, KAGEBAYASHI C, et al. Assessment of liver function in patients with hepatocellular carcinoma: A new evidence-based approach-the ALBI grade[J]. J Clin Oncol, 2015, 33( 6): 550- 558. DOI: 10.1200/JCO.2014.57.9151. [17] FUJITA K, OURA K, YONEYAMA H, et al. Albumin-bilirubin score indicates liver fibrosis staging and prognosis in patients with chronic hepatitis C[J]. Hepatol Res, 2019, 49( 7): 731- 742. DOI: 10.1111/hepr.13333. [18] YAMASHITA Y, UMEMURA T, KIMURA T, et al. Prognostic utility of albumin-bilirubin grade in Japanese patients with primary biliary cholangitis[J]. JHEP Rep, 2022, 5( 4): 100662. DOI: 10.1016/j.jhepr.2022.100662. [19] WANG J, ZHANG ZP, YAN XM, et al. Albumin-Bilirubin(ALBI) as an accurate and simple prognostic score for chronic hepatitis B-related liver cirrhosis[J]. Dig Liver Dis, 2019, 51( 8): 1172- 1178. DOI: 10.1016/j.dld.2019.01.011. [20] WANG YY, ZHONG JH, SU ZY, et al. Albumin-bilirubin versus Child-Pugh score as a predictor of outcome after liver resection for hepatocellular carcinoma[J]. Br J Surg, 2016, 103( 6): 725- 734. DOI: 10.1002/bjs.10095. [21] BAJAJ JS, RIDLON JM, HYLEMON PB, et al. Linkage of gut microbiome with cognition in hepatic encephalopathy[J]. Am J Physiol Gastrointest Liver Physiol, 2012, 302( 1): G168- G175. DOI: 10.1152/ajpgi.00190.2011. [22] JAIN L, SHARMA BC, SHARMA P, et al. Serum endotoxin and inflammatory mediators in patients with cirrhosis and hepatic encephalopathy[J]. Dig Liver Dis, 2012, 44( 12): 1027- 1031. DOI: 10.1016/j.dld.2012.07.002. [23] CHEN YH, YUAN W, MENG LK, et al. The role and mechanism of gut microbiota in pulmonary arterial hypertension[J]. Nutrients, 2022, 14( 20): 4278. DOI: 10.3390/nu14204278. [24] ISHIDA K, NAMISAKI T, MURATA K, et al. Accuracy of fibrosis-4 index in identification of patients with cirrhosis who could potentially avoid variceal screening endoscopy[J]. J Clin Med, 2020, 9( 11): 3510. DOI: 10.3390/jcm9113510. -



 PDF下载 ( 760 KB)
PDF下载 ( 760 KB)

 下载:
下载: