慢性胰腺炎并发区域性门静脉高压的影响因素及预测模型的构建
DOI: 10.12449/JCH240723
Influencing factors for chronic pancreatitis complicated by pancreatogenic portal hypertension and establishment of a predictive model
-
摘要:
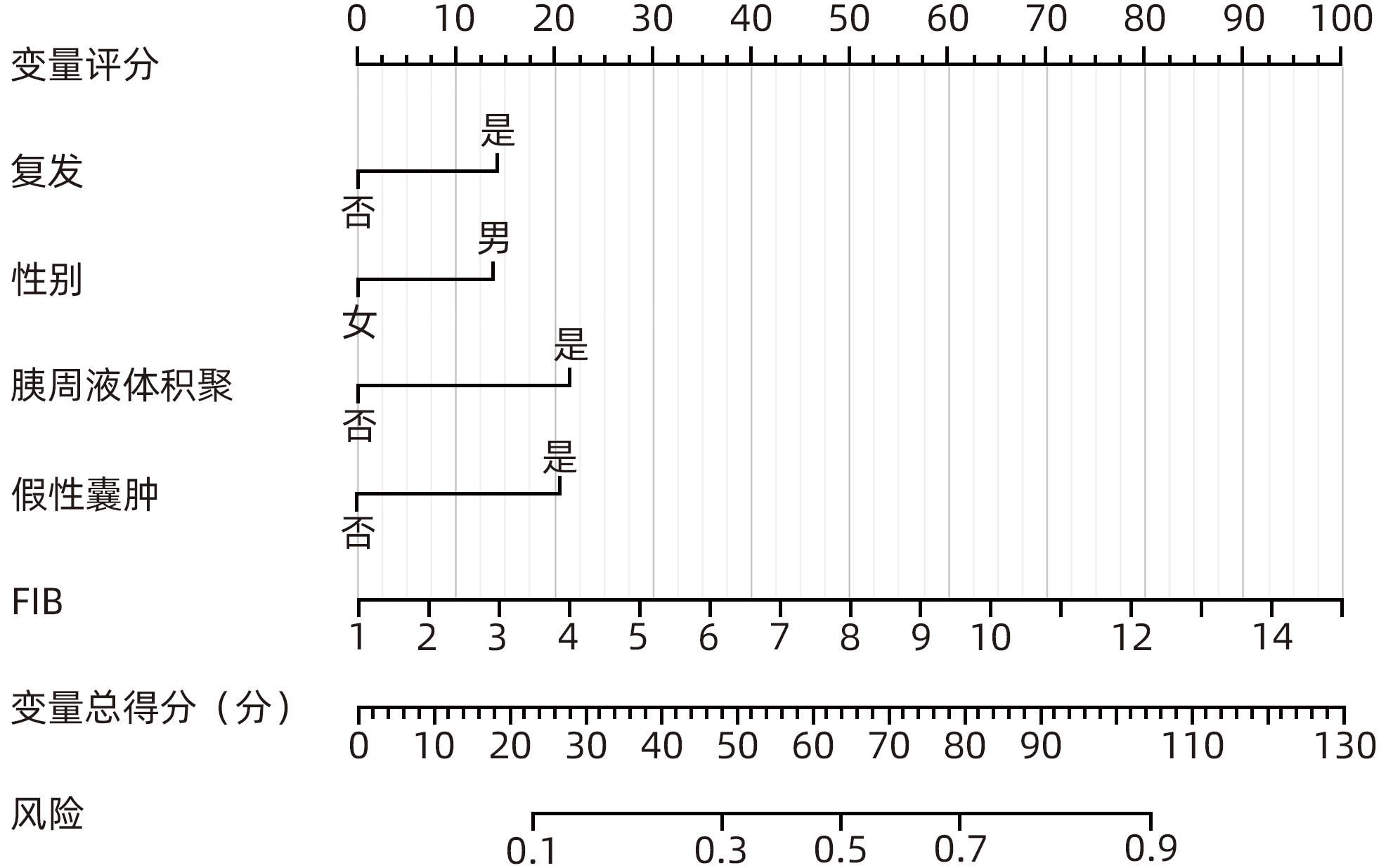
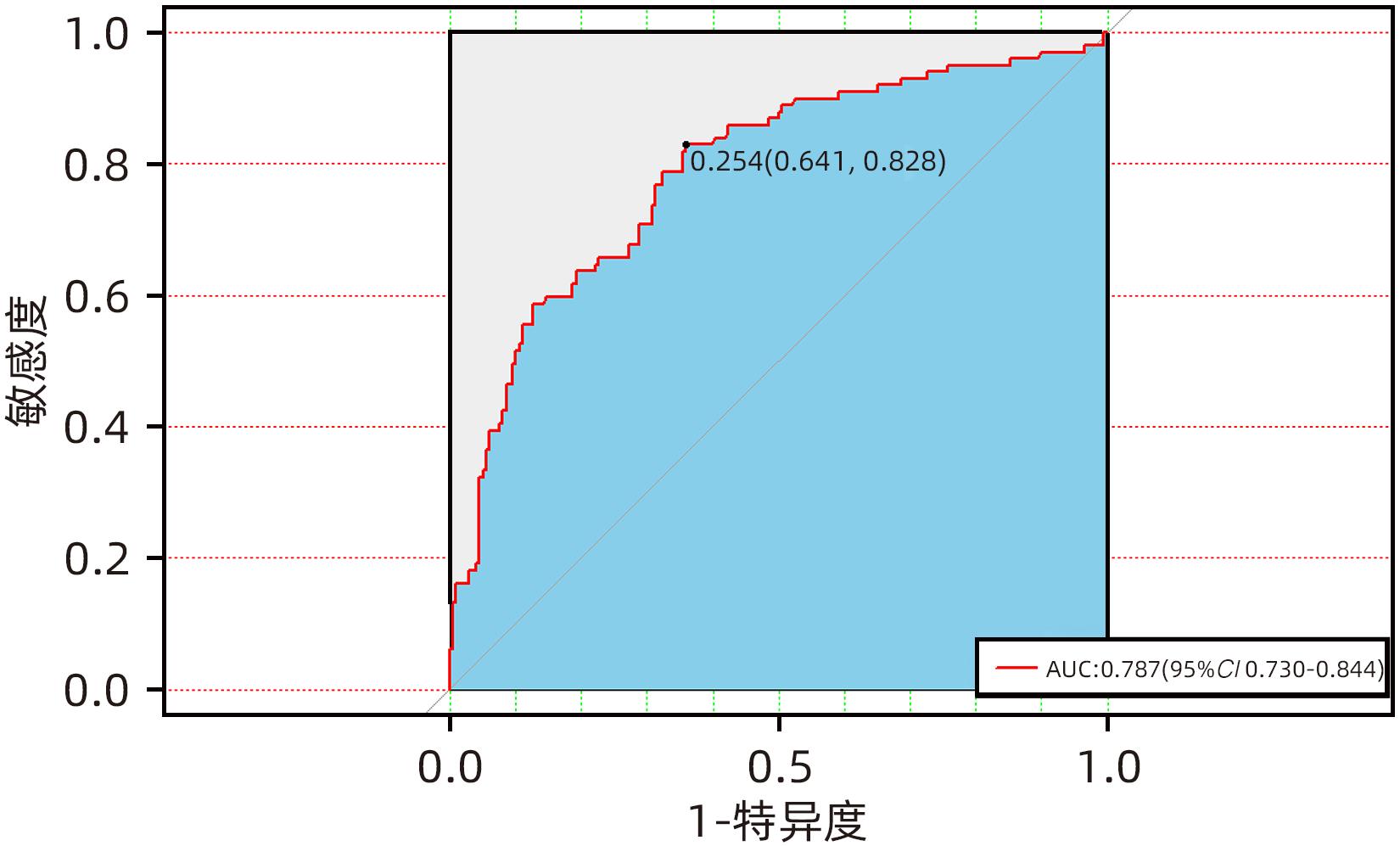
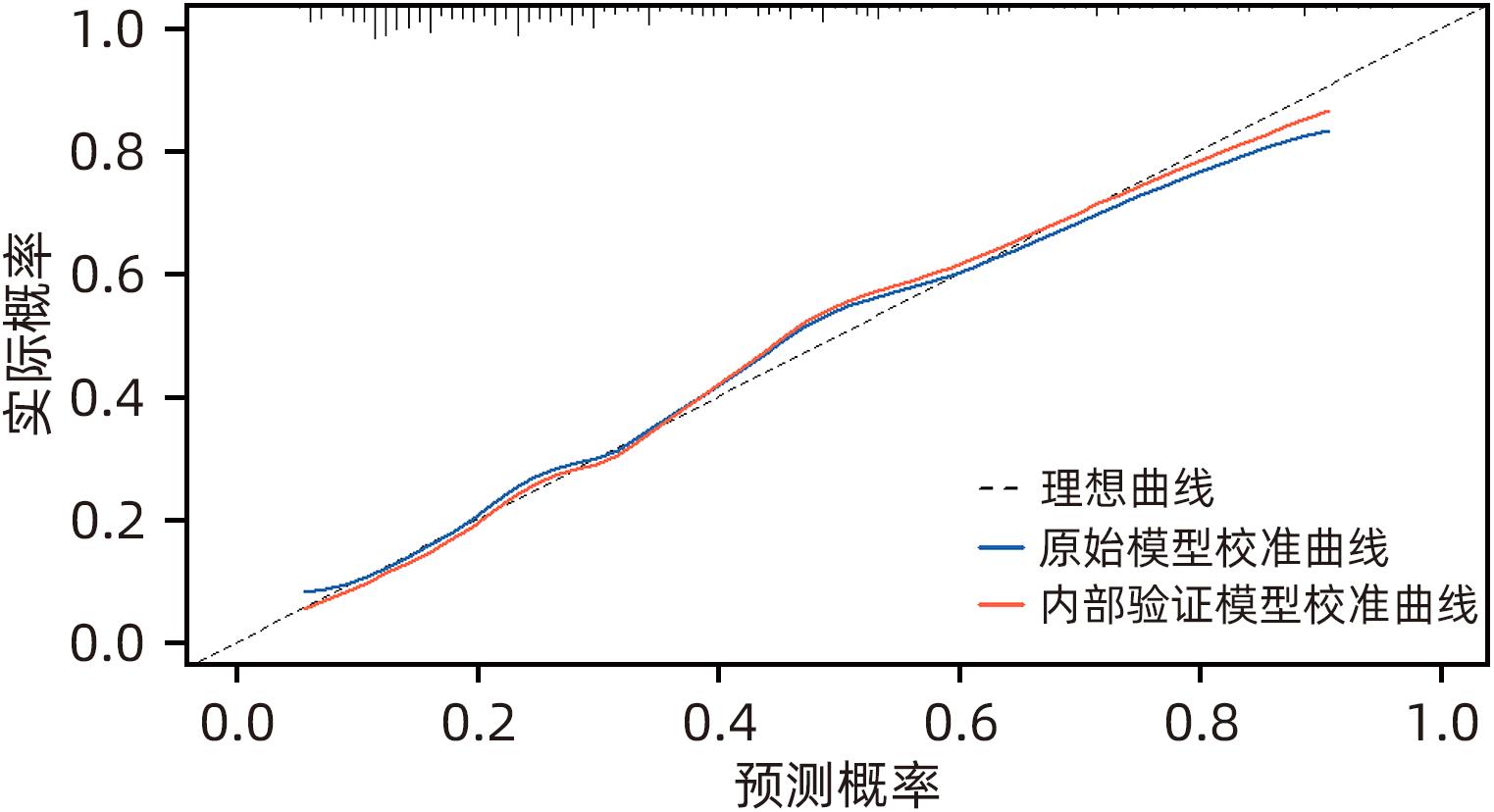
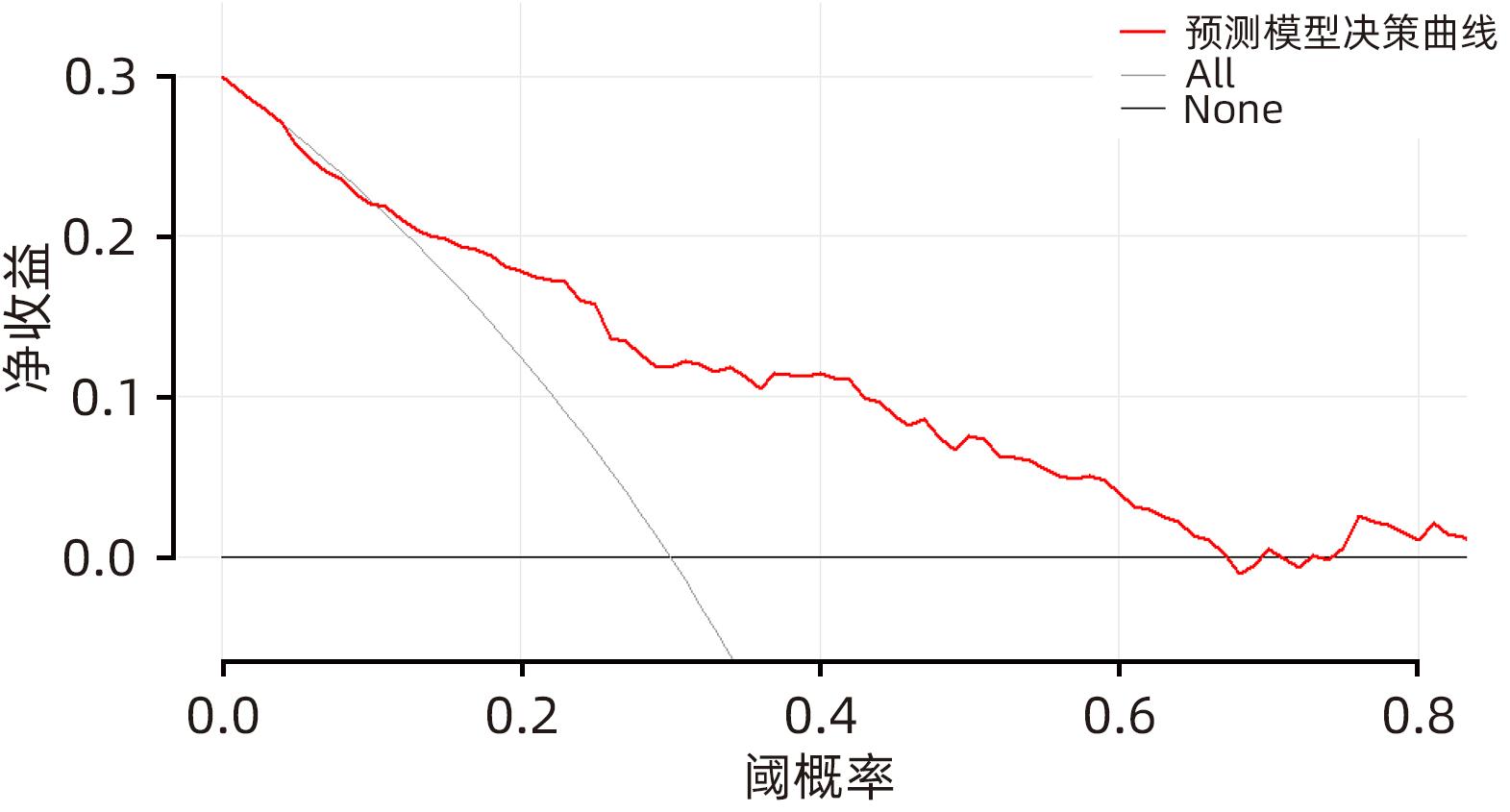
目的 探讨慢性胰腺炎(CP)并发区域性门静脉高压(PPH)的影响因素,并构建预测模型。 方法 回顾性分析2017年1月—2022年12月于昆明医科大学第一附属医院及楚雄彝族自治州人民医院、文山州人民医院、普洱市人民医院99例CP并发PPH(PPH组)住院患者的临床资料。采取发病率密度抽样法抽取198例CP患者作为对照组(非PPH组)。符合正态分布的计量资料两组间比较采用成组t检验;不符合正态分布的计量资料两组间比较采用Mann-Whitney U检验。计数资料两组间比较采用χ2检验或Fisher精确概率法。采用Lasso回归模型对CP并发PPH潜在的预测因子进行筛选,将筛选后的预测因子纳入多因素Logistic回归分析,筛选出独立危险因素,构建列线图;采用受试者工作特征曲线、校准曲线及Hosmer-Lemeshow拟合优度检验对模型进行内部验证;采用临床决策曲线评估模型的临床实用性。 结果 2组间性别、急性胰腺炎反复发作史、CP急性发作、胆管结石、胰周液体积聚、假性囊肿、肺部感染、C反应蛋白(CRP)升高占比、降钙素原升高占比、纤维蛋白原(FIB)、中性粒细胞与淋巴细胞比值(NLR)、GGT、TBil、DBil、低密度脂蛋白(LDL)、血清淀粉酶、D-二聚体、血清白蛋白比较差异均有统计学意义(P值均<0.05)。Lasso回归筛选的预测变量包括性别、急性胰腺炎反复发作、胆管结石、胰周液体积聚、肺部感染、假性囊肿、CRP、NLR、FIB、LDL。多因素Logistic回归分析显示,性别、急性胰腺炎反复发作、胰周液体积聚、假性囊肿、FIB是CP并发PPH的独立危险因素(OR值分别为2.716、2.138、2.297、2.805、1.313,P值均<0.05)。将上述因素进行模型拟合,经bootstrap内部验证列线图模型曲线下面积为0.787(95%CI:0.730~0.844),且校准曲线接近参考曲线,Hosmer-Lemeshow拟合优度检验表明该模型具有良好的拟合度(χ2=7.469,P=0.487)。临床决策曲线分析显示预测模型具有良好的临床实用性。 结论 男性、急性胰腺炎反复发作、胰周液体积聚、假性囊肿、FIB是CP并发PPH的独立危险因素,构建的列线图具有良好的区分度、校准度和临床实用性。 Abstract:Objective To investigate the influencing factors for chronic pancreatitis (CP) complicated by pancreatogenic portal hypertension (PPH), and to establish a predictive model. Methods A retrospective analysis was performed for the clinical data of 99 patients with CP complicated by PPH who were hospitalized in The First Affiliated Hospital of Kunming Medical University, Chuxiong Yi Autonomous Prefecture People’s Hospital, Wenshan People’s Hospital, and Puer People’s Hospital from January 2017 to December 2022, and these patients were enrolled as PPH group. The incidence density sampling method was used to select 198 CP patients from databases as control group. The independent-samples t test was used for comparison of normally distributed continuous data between two groups, and the Mann-Whitney U test was used for comparison of non-normally distributed continuous data between two groups; the chi-square test or the Fisher’s exact test was used for comparison of categorical data between two groups. The Least Absolute Shrinkage and Selection Operator (LASSO) regression model was used to identify the potential predictive factors for CP complicated by PPH, and the predictive factors obtained were included in the multivariate Logistic regression analysis to obtain independent risk factors, which were used to establish a nomogram prediction model. The receiver operating characteristic (ROC) curve, the calibration curve, and the Hosmer-Lemeshow goodness-of-fit test were used to perform internal validation of the model, and the clinical decision curve was used to assess the clinical practicability of the model. Results There were significant differences between the two groups in sex, history of recurrent acute pancreatitis attacks, acute exacerbation of CP, bile duct stones, peripancreatic fluid accumulation, pseudocysts, pulmonary infection, elevated C-reactive protein (CRP), elevated procalcitonin, fibrinogen (FIB), neutrophil-lymphocyte ratio (NLR), gamma-glutamyl transpeptidase, total bilirubin, direct bilirubin, low-density lipoprotein (LDL), serum amylase, D-dimer, and serum albumin (all P<0.05). The predictive variables obtained by the LASSO regression analysis included sex, recurrent acute pancreatitis attacks, bile duct stones, peripancreatic fluid accumulation, pulmonary infection, pseudocysts, CRP, NLR, FIB, and LDL. The multivariate Logistic regression analysis showed that sex (odds ratio [OR]=2.716, P<0.05), recurrent acute pancreatitis attacks (OR=2.138, P<0.05), peripancreatic fluid accumulation (OR=2.297, P<0.05), pseudocysts (OR=2.805, P<0.05), and FIB (OR=1.313, P<0.05) were independent risk factors for CP complicated by PPH. The above factors were fitted into the model, and the Bootstrap internal validation showed that the nomogram model had an area under the ROC curve of 0.787 (95% confidence interval: 0.730 — 0.844), and the calibration curve was close to the reference curve. The Hosmer-Lemeshow goodness-of-fit test showed that the model had a good degree of fitting (χ2=7.469, P=0.487). The clinical decision curve analysis showed that the prediction model had good clinical practicability. Conclusion Male sex, recurrent acute pancreatitis attacks, peripancreatic fluid accumulation, pseudocysts, and FIB are independent risk factors for CP complicated by PPH, and the nomogram model established has good discriminatory ability, calibration, and clinical practicability. -
表 1 两组患者一般资料比较
Table 1. Comparison of general data between the two groups
临床指标 PPH组(n=99) 非PPH组(n=198) 统计值 P值 性别[例(%)] χ2=7.913 0.005 男 89(89.9) 151(76.3) 女 10(10.1) 47(23.7) 年龄(岁) 46.61±13.29 49.30±15.46 t=-1.483 0.139 发病年龄(岁) 45.61±13.43 47.52±15.56 t=-1.023 0.307 诊断年龄(岁) 47.10±12.76 48.66±15.27 t=-0.860 0.390 BMI(kg/m2) 21.00±3.12 20.63±2.90 t=1.107 0.310 既往史[例(%)] 糖尿病病史 17(17.2) 38(19.2) χ2=0.179 0.673 高血压病史 9(9.1) 24(12.1) χ2=0.614 0.433 胆囊切除术后 13(13.1) 25(12.6) χ2=0.015 0.902 急性胰腺炎反复发作 68(68.7) 107(54.0) χ2=5.850 0.016 吸烟史[例(%)] 38(38.4) 63(31.8) χ2=1.797 0.180 饮酒量[例(%)] χ2=3.160 0.368 不饮酒 52(52.5) 118(59.6) 0~20 g/d 1(1.0) 6(3.0) >20~80 g/d 11(11.1) 16(8.1) >80 g/d 35(35.4) 58(29.3) CP急性发作[例(%)] 68(68.7) 101(51.0) χ2=8.409 0.004 M-ANNHEIM临床分期[例(%)] χ2=1.194 0.762 Ⅰ期 61(61.6) 130(65.7) Ⅱ期 34(34.3) 57(28.8) Ⅲ期 3(3.0) 7(3.5) Ⅳ期 1(1.0) 4(2.0) 体质量减轻[例(%)] 31(31.3) 76(38.4) χ2=1.432 0.231 住院时间(d) 9.00(7.00~14.00) 9.00(6.00~14.00) Z=-0.865 0.387 住院费用(元) 13 664.54(8 388.05~24 598.10) 10 896.15(6 932.75~32 775.60) Z=-0.818 0.414 表 2 两组患者实验室指标及并发症比较
Table 2. Comparison of laboratory data and complication between the two groups
临床指标 PPH组(n=99) 非PPH组(n=198) 统计值 P值 NLR 4.47(2.41~9.25) 2.01(1.49~3.25) Z=-5.882 <0.001 PLR 152.10(101.97~209.62) 127.00(97.16~187.78) Z=-0.954 0.340 HCT 0.41(0.37~0.44) 0.41(0.38~0.45) Z=-1.324 0.185 PDW 13.45(11.50~14.75) 12.60(11.10~14.53) Z=-1.686 0.092 CRP升高[例(%)] 59(59.6) 50(25.3) χ2=33.509 <0.001 PCT升高[例(%)] 25(25.3) 21(10.6) χ2=10.817 0.001 ALT(U/L) 22.00(13.14~42.50) 26.05(17.68~44.13) Z=-1.462 0.144 AST(U/L) 19.00(13.08~40.09) 22.85(16.63~35.00) Z=-1.879 0.060 ALP(U/L) 83.85(63.15~109.90) 77.95(63.78~108.03) Z=-0.813 0.416 GGT(U/L) 38.90(20.50~138.57) 28.50(15.00~88.00) Z=-2.311 0.021 TBil(μmol/L) 14.25(9.80~22.08) 10.80(7.45~14.65) Z=-3.799 <0.001 DBil(μmol/L) 5.70(3.55~9.45) 4.40(3.40~6.13) Z=-2.226 0.026 BUN(mmol/L) 4.46(3.57~5.84) 4.66(3.71~5.82) Z=-0.379 0.705 SCr(μmol/L) 73.85(59.75~89.23) 74.95(64.05~85.33) Z=-0.451 0.652 TC(mmol/L) 3.58±1.41 3.82±1.06 t=-1.658 0.098 LDL(mmol/L) 1.94±0.64 2.24±0.82 t=-3.210 0.001 TG(mmol/L) 1.28(0.89~1.81) 1.19(0.84~1.79) Z=-1.046 0.295 血淀粉酶(U/L) 111.50(54.30~304.00) 67.50(50.00~133.30) Z=-2.950 0.003 TT(s) 17.20(16.10~18.80) 17.70(16.50~18.90) Z=-1.348 0.178 INR 1.09±0.11 1.08±0.15 t=0.526 0.599 FIB(g/L) 3.96(3.00~5.36) 3.10(2.61~4.08) Z=-4.672 <0.001 DD2(mg/L) 0.96(0.32~2.50) 0.30(0.15~1.06) Z=-4.716 <0.001 Alb(g/L) 37.76±6.29 39.84±5.58 t=-2.896 0.004 Ca2+(mmol/L) 2.24(2.13~2.36) 2.28(2.19~2.39) Z=-1.946 0.520 并发症[例(%)] 胰周淋巴结肿大 21(21.2) 40(20.2) χ2=0.041 0.839 胰周液体积聚 37(37.4) 24(12.1) χ2=25.788 <0.001 假性囊肿 44(44.4) 30(15.2) χ2=30.272 <0.001 十二指肠梗阻 7(7.1) 9(4.5) χ2=0.826 0.364 胰瘘 2(3.2) 1(0.8) χ2=0.381 0.537 胆管结石 38(38.4) 44(22.2) χ2=8.625 0.003 假性动脉瘤 1(1.0) 0(0.0) χ2=2.007 0.333 胆总管狭窄 9(9.1) 8(4.0) χ2=3.120 0.077 肺部感染 23(23.2) 16(8.1) χ2=13.283 <0.001 肝损伤 27(27.3) 42(21.2) χ2=1.359 0.244 肾损伤 5(5.1) 10(5.1) χ2=0.000 >0.05 脾梗死 7(7.1) 20(10.1) χ2=0.733 0.392 表 3 CP并发PPH多因素Logistic回归分析
Table 3. Multivariate Logistic regression analysis of PPH in patients with CP
变量 P值 OR 95%CI 性别 0.024 2.716 1.139~6.480 急性胰腺炎反复 发作史(复发) 0.016 2.138 1.152~3.968 胆管结石 0.065 1.185 0.964~3.419 假性囊肿 0.001 2.805 1.485~5.298 胰周液体积聚 0.018 2.297 1.153~4.577 肺部感染 0.478 1.363 0.580~3.202 CRP 0.166 1.596 0.824~3.090 LDL 0.159 0.751 0.504~1.118 NLR 0.056 1.072 0.998~1.152 FIB 0.014 1.313 1.057~1.631 -
[1] Chronic Pancreatitis Group of Pancreatic Disease Committee of Chinese Medical Doctor Association. Guideline for the diagnosis and treatment of chronic pancreatitis(2018, Guangzhou)[J]. J Clin Hepatol, 2019, 35( 1): 45- 51. DOI: 10.3969/j.issn.1001-5256.2019.01.008.中国医师协会胰腺病专业委员会慢性胰腺炎专委会. 慢性胰腺炎诊治指南(2018, 广州)[J]. 临床肝胆病杂志, 2019, 35( 1): 45- 51. DOI: 10.3969/j.issn.1001-5256.2019.01.008. [2] ADAM U, MAKOWIEC F, RIEDIGER H, et al. Pancreatic head resection for chronic pancreatitis in patients with extrahepatic generalized portal hypertension[J]. Surgery, 2004, 135( 4): 411- 418. DOI: 10.1016/j.surg.2003.08.021. [3] RU N, HE CH, REN XL, et al. Risk factors for sinistral portal hypertension and related variceal bleeding in patients with chronic pancreatitis[J]. J Dig Dis, 2020, 21( 8): 468- 474. DOI: 10.1111/1751-2980.12916. [4] LATORRE FRAGUA RA, MANUEL VÁZQUEZ A, LÓPEZ MARCANO AJ, et al. Pancreatic surgery in chronic pancreatitis complicated by extrahepatic portal hypertension or cavernous transformation of the portal vein: A systematic review[J]. Scand J Surg, 2020, 109( 3): 177- 186. DOI: 10.1177/1457496919857260. [5] KUL M, NÜ HALILOĞLU, HÜRSOY N, et al. Sinistral portal hypertension: Computed tomography imaging findings and clinical appearance-a descriptive case series[J]. Can Assoc Radiol J, 2018, 69( 4): 417- 421. DOI: 10.1016/j.carj.2018.07.006. [6] PEREIRA P, PEIXOTO A. Left-sided portal hypertension: A clinical challenge[J]. GE Port J Gastroenterol, 2015, 22( 6): 231- 233. DOI: 10.1016/j.jpge.2015.10.001. [7] YU DJ, LI XL, GONG JP, et al. Left-sided portal hypertension caused by peripancreatic lymph node tuberculosis misdiagnosed as pancreatic cancer: A case report and literature review[J]. BMC Gastroenterol, 2020, 20( 1): 276. DOI: 10.1186/s12876-020-01420-x. [8] FERNANDES A, ALMEIDA N, FERREIRA AM, et al. Left-sided portal hypertension: A sinister entity[J]. GE Port J Gastroenterol, 2015, 22( 6): 234- 239. DOI: 10.1016/j.jpge.2015.09.006. [9] PATEL H, BHANDARI P, KUMAR K, et al. Isolated gastric varices due to essential thrombocytosis related to splenic vein thrombosis: A challenge to uncover the concealed diagnosis[J]. Cureus, 2019, 11( 11): e6068. DOI: 10.7759/cureus.6068. [10] ZHENG KX, GUO XZ, FENG J, et al. Gastrointestinal bleeding due to pancreatic disease-related portal hypertension[J]. Gastroenterol Res Pract, 2020, 2020: 3825186. DOI: 10.1155/2020/3825186. [11] XIE CL, WU CQ, CHEN Y, et al. Sinistral portal hypertension in acute pancreatitis: A magnetic resonance imaging study[J]. Pancreas, 2019, 48( 2): 187- 192. DOI: 10.1097/MPA.0000000000001242. [12] ZHAO YP, LI XB, LI HW, et al. Diagnosis and treatment guidelines for pancreatic portal hypertension(draft)[J]. Chin J Gen Surg, 2013, 28( 5): 405- 406. DOI: 10.3760/cma.j.issn.1007-631X.2013.05.032.赵玉沛, 李晓斌, 李宏为, 等. 胰源性门静脉高压症诊治规范(草案)[J]. 中华普通外科杂志, 2013, 28( 5): 405- 406. DOI: 10.3760/cma.j.issn.1007-631X.2013.05.032. [13] TALAGALA IA, NAWARATHNE M, ARAMBEPOLA C. Novel risk factors for primary prevention of oesophageal carcinoma: A case-control study from Sri Lanka[J]. BMC Cancer, 2018, 18( 1): 1135. DOI: 10.1186/s12885-018-4975-4. [14] KÖKLÜ S, ÇOBAN Ş, YÜKSEL O, et al. Left-sided portal hypertension[J]. Dig Dis Sci, 2007, 52( 5): 1141- 1149. DOI: 10.1007/s10620-006-9307-x. [15] PAN YM, XIE M, BAO SH, et al. The diagnosis and treatment of pancreatic segmental portal hypertension with upper gastrointestinal bleeding[J]. J Clin Hepatol, 2011, 27( 11): 1184- 1186. DOI: 10.3969/j.issn.1001-5256.2011.11.011.潘一明, 谢敏, 包善华, 等. 胰源性区域性门脉高压症合并上消化道出血的诊治分析[J]. 临床肝胆病杂志, 2011, 27( 11): 1184- 1186. DOI: 10.3969/j.issn.1001-5256.2011.11.011. [16] TU GP, SUN JC, LIU YF, et al. Clinical experience of pancreatitis causing regional portal hypertension of pancreatic origin[J]. J Hepatobiliary Surg, 2019, 27( 6): 418- 422. DOI: 10.3969/j.issn.1006-4761.2019.06.007.涂广平, 孙吉春, 刘云飞, 等. 胰腺炎引起胰源性区域性门脉高压临床诊疗经验探讨[J]. 肝胆外科杂志, 2019, 27( 6): 418- 422. DOI: 10.3969/j.issn.1006-4761.2019.06.007. [17] LI ZS, GUO HL. Progress in diagnosis and treatment of pancreatic portal hypertension[J]. J Hepatobiliary Surg, 2017, 25( 5): 325- 328. DOI: 10.3969/j.issn.1006-4761.2017.05.003.李兆申, 郭洪雷. 胰源性门脉高压症的诊治进展[J]. 肝胆外科杂志, 2017, 25( 5): 325- 328. DOI: 10.3969/j.issn.1006-4761.2017.05.003. [18] KININY W EL, KEARNEY L, HOSAM N, et al. Recurrent variceal haemorrhage managed with splenic vein stenting[J]. Ir J Med Sci, 2017, 186( 2): 323- 327. DOI: 10.1007/s11845-016-1420-z. [19] IRAWAN H, MULYAWAN IM. Combination of modified Sugiura technique and proximal splenorenal shunt for the management of portal vein thrombosis in noncirrhotic portal hypertension[J]. Clin Exp Gastroenterol, 2019, 12: 149- 156. DOI: 10.2147/CEG.S188200. [20] WANI ZA, BHAT RA, BHADORIA AS, et al. Extrahepatic portal vein obstruction and portal vein thrombosis in special situations: Need for a new classification[J]. Saudi J Gastroenterol, 2015, 21( 3): 129- 138. DOI: 10.4103/1319-3767.157550. [21] YU C, DING L, JIANG ML, et al. Dynamic changes and nomogram prediction for sinistral portal hypertension in moderate and severe acute pancreatitis[J]. Front Med, 2022, 9: 875263. DOI: 10.3389/fmed.2022.875263. [22] EASLER J, MUDDANA V, FURLAN A, et al. Portosplenomesenteric venous thrombosis in patients with acute pancreatitis is associated with pancreatic necrosis and usually has a benign course[J]. Clin Gastroenterol Hepatol, 2014, 12( 5): 854- 862. DOI: 10.1016/j.cgh.2013.09.068. [23] LI H, YANG ZY, TIAN F. Clinical characteristics and risk factors for sinistral portal hypertension associated with moderate and severe acute pancreatitis: A seven-year single-center retrospective study[J]. Med Sci Monit, 2019, 25: 5969- 5976. DOI: 10.12659/MSM.916192. [24] RAMSEY ML, CONWELL DL, HART PA. Complications of chronic pancreatitis[J]. Dig Dis Sci, 2017, 62( 7): 1745- 1750. DOI: 10.1007/s10620-017-4518-x. [25] BALAKRISHNAN V, UNNIKRISHNAN AG, THOMAS V, et al. Chronic pancreatitis. A prospective nationwide study of 1, 086 subjects from India[J]. JOP, 2008, 9( 5): 593- 600. [26] PANDEY V, PATIL M, PATEL R, et al. Prevalence of splenic vein thrombosis and risk of gastrointestinal bleeding in chronic pancreatitis patients attending a tertiary hospital in western India[J]. J Family Med Prim Care, 2019, 8( 3): 818- 822. DOI: 10.4103/jfmpc.jfmpc_414_18. [27] HAO L, PAN J, WANG D, et al. Risk factors and nomogram for pancreatic pseudocysts in chronic pancreatitis: A cohort of 1998 patients[J]. J Gastroenterol Hepatol, 2017, 32( 7): 1403- 1411. DOI: 10.1111/jgh.13748. [28] ZHANG C, LIN T, ZHANG JY, et al. Diagnosis and treatment of acute pancreatitis complicated with regional portal hypertension[J/OL]. Chin J Hepatic Surg Electron Ed, 2022, 11( 1): 48- 53. DOI: 10.3877/cma.j.issn.2095-3232.2022.01.011.张春, 林婷, 张靖垚, 等. 急性胰腺炎合并区域性门静脉高压症诊治分析[J/OL]. 中华肝脏外科手术学电子杂志, 2022, 11( 1): 48- 53. DOI: 10.3877/cma.j.issn.2095-3232.2022.01.011. [29] YANG Y, WANG YZ, LI YJ, et al. Analysis of risk factors for acute pancreatitis with thrombotic diseases[J]. Chin J Pancreatol, 2021, 21( 4): 258- 263. DOI: 10.3760/cma.j.cn115667-20210411-00076.杨颖, 王鵷臻, 李亚俊, 等. 急性胰腺炎并发血栓性疾病的危险因素分析[J]. 中华胰腺病杂志, 2021, 21( 4): 258- 263. DOI: 10.3760/cma.j.cn115667-20210411-00076. [30] LIU KJ, CHEN DF. Diagnosis and treatment of hypercoagulability in severe acute pancreatitis[J]. Chin J Pancreatol, 2017, 17( 2): 73- 76. DOI: 10.3760/cma.j.issn.1674-1935.2017.02.001.刘凯军, 陈东风. 重症急性胰腺炎血液高凝状态的诊断和治疗[J]. 中华胰腺病杂志, 2017, 17( 2): 73- 76. DOI: 10.3760/cma.j.issn.1674-1935.2017.02.001. [31] MACHLUS KR, CARDENAS JC, CHURCH FC, et al. Causal relationship between hyperfibrinogenemia, thrombosis, and resistance to thrombolysis in mice[J]. Blood, 2011, 117( 18): 4953- 4963. DOI: 10.1182/blood-2010-11-316885. [32] WOLBERG AS, SANG YQ. Fibrinogen and factor XIII in venous thrombosis and Thrombus stability[J]. Arterioscler Thromb Vasc Biol, 2022, 42( 8): 931- 941. DOI: 10.1161/ATVBAHA.122.317164. [33] FEI Y, GAO K, HU J, et al. Predicting the incidence of portosplenomesenteric vein thrombosis in patients with acute pancreatitis using classification and regression tree algorithm[J]. J Crit Care, 2017, 39: 124- 130. DOI: 10.1016/j.jcrc.2017.02.019. [34] TOQUÉ L, HAMY A, HAMEL JF, et al. Predictive factors of splanchnic vein thrombosis in acute pancreatitis: A 6-year single-center experience[J]. J Dig Dis, 2015, 16( 12): 734- 740. DOI: 10.1111/1751-2980.12298. -



 PDF下载 ( 1040 KB)
PDF下载 ( 1040 KB)


 下载:
下载: