Chinese expert consensus on clinical management of hepatopathy-related thrombocytopenia
-
摘要: 肝病相关血小板减少症指肝病或肝病治疗所致的血小板减少症,发生率与肝病病程及严重程度相关。血小板减少症对肝病患者临床结局的直接影响是出血风险增加,间接影响涉及因潜在出血风险导致的治疗延迟或终止。肝病相关血小板减少症的病理生理机制涉及血小板生成减少、分布异常、破坏或消耗增加等。目前,针对不同机制的治疗策略包括促血小板生成药物、手术、免疫抑制药物及输注血小板等,但临床应用有待进一步规范。为提升我国肝病相关血小板减少症在诊断、分型及治疗方案合理选择等方面的临床管理水平,国家感染性疾病临床医学研究中心组织专家,参考领域最新循证医学证据,讨论制定了本共识。Abstract: Hepatopathy-related thrombocytopenia refers to a decrease in platelet count caused by liver disease or its treatment, and the incidence rate of this disease is associated with the course and severity of liver disease. The direct effect of thrombocytopenia on the clinical outcome of patients with liver disease is an increased risk of bleeding, and its indirect effect involves delay or discontinuation of treatment due to the potential risk of bleeding. The pathophysiological mechanisms of hepatopathy-related thrombocytopenia involve reduced platelet production, abnormal platelet distribution, and increased destruction or consumption. Current treatment strategies aiming at different mechanisms include thrombopoietic agents, surgery, immunosuppressants, and platelet transfusion, but their clinical application needs further standardization. In order to improve the clinical management of hepatopathy-related thrombocytopenia in China in terms of diagnosis, typing, and rational selection of treatment regimens, National Clinical Research Center for Infectious Diseases organized experts to discuss and develop these consensus statements with reference to the latest evidence of evidence-based medicine in this field.
-
Key words:
- Liver Diseases /
- Thrombocytopenia /
- Consensus
-
慢性肝病患者中血小板减少症(thrombocytopenia,TP)的患病率非常高,其中慢性肝炎患者TP患病率为6%~16%,肝硬化患者TP患病率高达78%[1]。最常见的肝炎病毒相关TP是由于肝脏病变、脾脏病变、免疫破坏和骨髓抑制等因素导致血小板(platelet,PLT)生成减少和破坏增加,最终导致TP[2]。而对于肝脏肿瘤患者,除肝病本身外,肿瘤治疗会进一步加剧血小板减少,如接受经肝动脉化疗栓塞术(transarterial chemoembolization,TACE)治疗患者TP发生率为21.3%,≥3级者为2%[3],接受索拉非尼或索拉非尼联合肝动脉化疗灌注术(hepatic artery infusion chemotherapy,HAIC)治疗的患者≥3级TP发生率分别为12.0%和34.0%[4]。TP与肝病患者诸多不良结局密切相关,如肝切除术后肝衰竭、有创操作相关出血、肝纤维化进展等[5]。尽管现有多项指南/共识对TP管理提出推荐意见,但尚缺乏针对肝病相关TP的系统性诊疗推荐。本共识聚焦肝病相关TP,全面梳理相关病理生理机制、诊断、分型及治疗文献,结合专家经验,总结归纳出临床诊疗细则,旨在为肝病相关TP的规范化诊疗提供参考。
1. 方法学
通过对PubMed数据库、中国知网、万方等数据库进行了检索,获得肝病相关血小板减少的关键文献,检索关键词包括:liver disease、thrombocytopenia、肝病、血小板减少症等。在共识制定会议期间,共识专家组成员筛选和评估了用于审阅的重要数据,基于证据级别和专家意见,通过专家投票最终形成13条推荐意见。本共识推荐级别及其代表意义见表1。
表 1 推荐级别及定义Table 1. Recommendation grades and definitions推荐级别 代表意义 1类 基于高级别临床证据,专家意见高度一致 2A类 基于低级别临床证据,专家意见高度一致;或基于高级别证据,专家意见基本一致 2B类 基于低级别临床证据,专家意见基本一致 3类 不论基于何种级别临床证据,专家意见明显分歧 2. 定义
肝病相关血小板减少症(hepatopathy-related thrombopenia,HRT)是指各种急慢性肝病患者(包括急慢性病毒性肝炎、药物性肝炎、酒精性肝病、非酒精性脂肪性肝病、自身免疫性肝病、代谢性肝病、隐源性肝病及肝脏肿瘤等)在疾病发展过程中,因肝病本身或肝病相关治疗所致的血小板减少,国际上定义为血小板计数低于150×109/L,国内通常定义为血小板计数低于100×109/L[6-7]。
推荐意见1:HRT定义:因肝病或肝病相关治疗所致的血小板计数低于100×109/L(推荐级别:2A)。
3. 病理生理机制
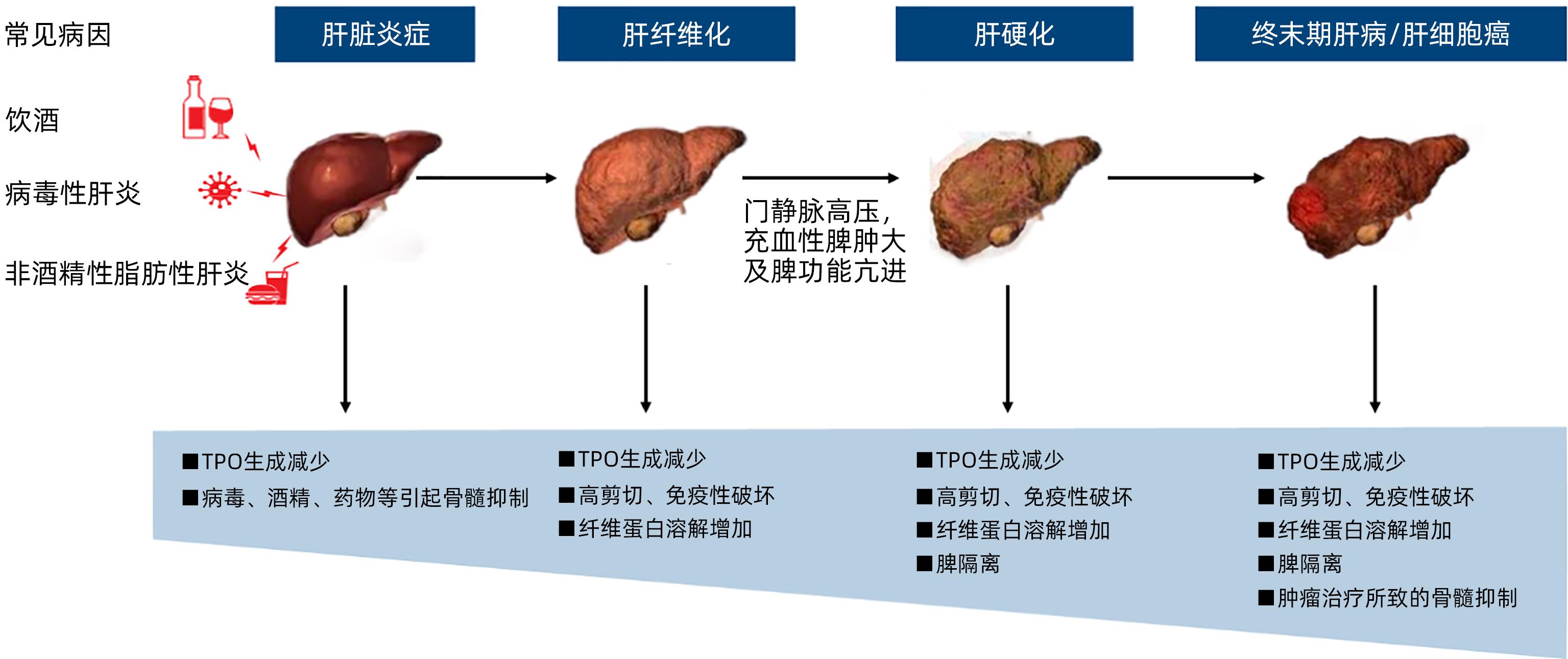
HRT是一个多因素参与的复杂病理生理过程,涉及多种机制:包括血小板生成减少、破坏增加、分布异常和消耗增加等。
血小板生成素(thrombopoietin,TPO)主要由肝实质细胞和肝窦内皮细胞产生,是调节巨核细胞增殖分化、成熟和介导血小板生成的主要细胞因子。肝病患者由于肝细胞破坏导致TPO分泌减少,TPO水平降低,成熟巨核细胞数量减少、血小板生成减少。病毒(HAV、HBV、HCV等)、药物(硫唑嘌呤、β-内酰胺类抗生素、氟喹诺酮类抗生素、干扰素、奥沙利铂、卡铂、吉西他滨等)可引起骨髓巨核细胞成熟障碍或生成减少导致血小板生成不足。
约64%慢性肝病患者可产生抗血小板抗体,引起免疫性血小板破坏[8];肝硬化脾肿大,脾内巨噬细胞数量增加、吞噬能力增强,导致血小板破坏增加[9];肝硬化引起脉管系统内剪切力增加,高剪切力状态下血管性血友病因子(von Willebrand Factor,vWF)从球状构象转变为对血小板更具黏附性的长链构象,引起血小板过度聚集,也会使血小板破坏增加[10]。
血小板减少还与血小板分布异常有关。肝硬化门静脉高压患者脾脏血液回流受阻,脾脏瘀血肿大[11],滞留在脾脏血管池内的血小板数量明显增加。在脾脏极度肿大的情况下,脾脏内的外周血血小板滞留百分比可由生理状态下的30%增加至90%,导致外周血血小板计数明显下降[9]。
此外,肝硬化时纤维蛋白溶解增加,凝血和抑制因子产生减少,血管内凝血加速,血小板过度消耗。肝病患者接受手术操作,如经肝动脉介入、局部消融、肝切除等,会增加出血风险,引起血小板消耗增加(图1)。
推荐意见2:HRT的发生与肝病病因、病程、严重程度等多种因素相关,机制涉及TPO生成减少、血小板破坏增加和血小板分布异常、骨髓抑制等;了解这些病理生理机制,是HRT临床诊治的基础(推荐级别:2A)。
4. 诊断及鉴别诊断
4.1 血小板功能检测
血小板功能检测用于辅助诊断血小板相关疾病及抗血小板聚集治疗疗效监测,常用检测指标包括:TPO水平、血栓弹力图(thromboelastography,TEG)、血小板抗体等[12](表2)。
表 2 血小板功能相关检测Table 2. Platelet function related tests指标 检测设备 标本 正常值 临床意义 TPO水平检测 离心机、37 ℃恒温水浴箱、酶标仪、移液器、洗板机等 血清样本或血浆(EDTA或柠檬酸钠或肝素抗凝)样本均可 最广泛使用的ELISA法测定的正常值为(64±41)pg/mL(范围27~188 pg/mL) 根据《成人原发免疫性血小板减少症诊断与治疗中国指南(2020年版)》,血清TPO水平测定的意义:(1)鉴别不典型再生障碍性贫血(AA)、低增生骨髓增生异常综合征;(2)用于常规治疗无效患者及脾切除前疾病重新评估 TEG TEG仪(检测方法按仪器说明书进行操作) 动脉血或静脉血均可 参考医院提供的实验室检查正常值范围标准 凝血因子定性分析、纤维蛋白原的定性分析、血小板数量与质量的定性分析、检测血液中是否有肝素的影响、测定纤溶活性、诊断高凝状态、判断血栓风险、鉴别术后渗血和出血、准确判断原因、诊断弥散性血管内凝血(DIC)、监测体外循环和心脏介入治疗等的抗凝情况、监测肝移植手术的出血及凝血状态,以及监测抗血小板药物治疗效果和并发症等 血小板抗体检查 离心机、恒温水浴箱、酶标仪、移液器、振荡器等 血清样本或血浆(EDTA或枸橼酸钠抗凝)样本均可 结果判定:阴性 用途:(1)人类血小板抗原(HPA)抗体检测;(2)HPA型。 根据《成人原发免疫性血小板减少症诊断与治疗中国指南(2020年版)》,血小板糖蛋白特异性自身抗体检查的意义:(1)鉴别非免疫性血小板减少;(2)常规治疗无效患者及脾切除前疾病重新评估;(3)指导静脉注射人免疫球蛋白治疗 注:EDTA,乙二胺四乙酸。 推荐意见3:TPO水平、TEG、血小板抗体等3种血小板功能性检测指标可作为鉴别诊断TP的主要参考依据(推荐级别:2B)。
4.2 诊断及鉴别诊断
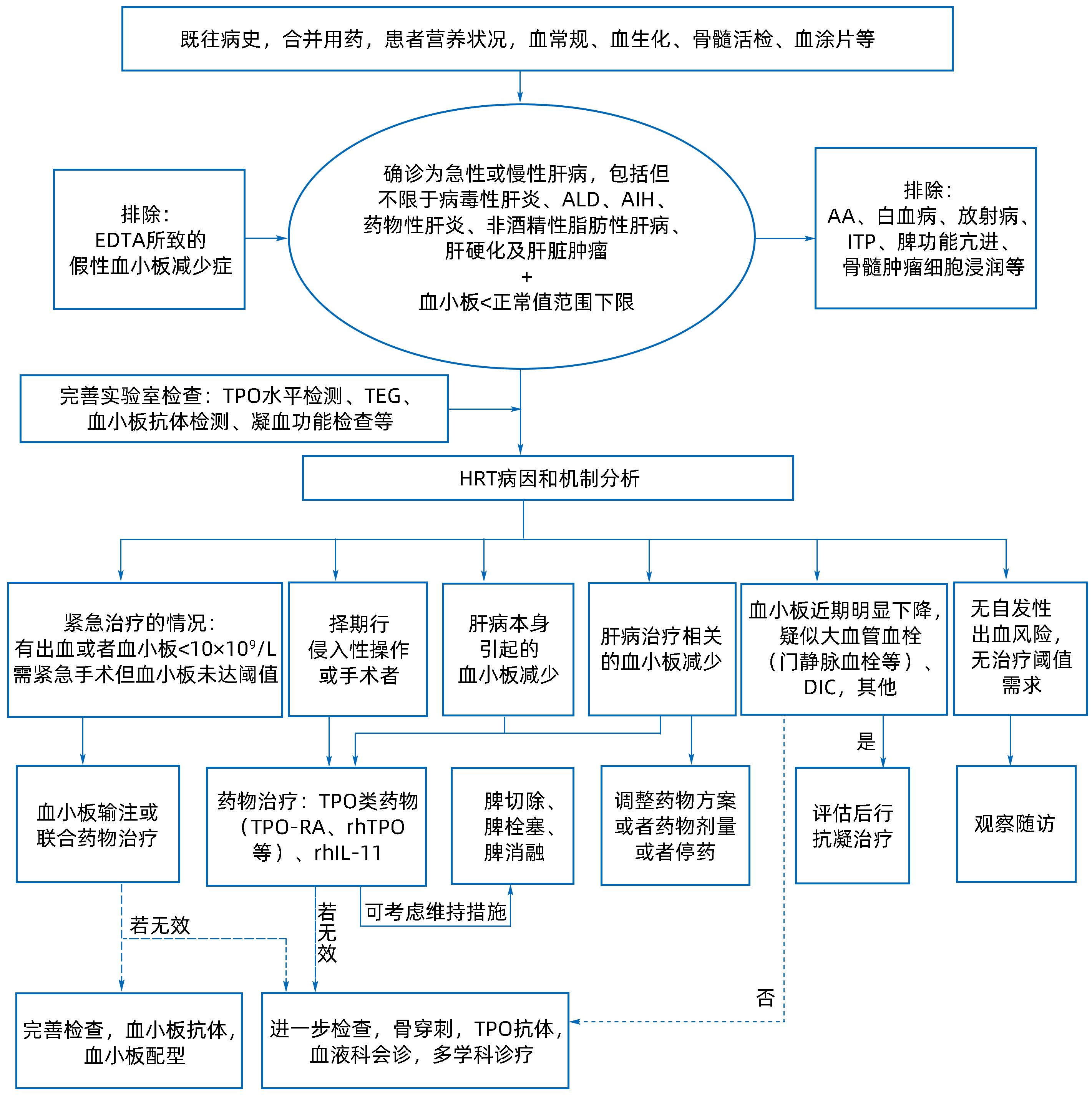
HRT的临床诊断标准包含下述要点:(1)外周血血小板计数<100×109/L;(2)合并有病毒性肝病、酒精性肝病、非酒精性脂肪性肝病、自身免疫性肝病、药物性肝病、代谢性肝病、隐源性肝病、原发性肝癌等基础肝脏疾病[13-14];(3)排除其他基础疾病和/或导致TP的合并症,如AA、白血病、放射病、原发免疫性血小板减少症(primary immune thrombocytopenia,ITP)、骨髓肿瘤细胞浸润等;(4)排除EDTA抗凝剂所致的假性TP。
其他情况如血液系统疾病、免疫性疾病、感染性疾病、肿瘤治疗、药物使用、妊娠期特殊状态、输血等亦可引起TP[15]。因此,临床诊疗中需详细了解患者血小板减少的背景,通过完善实验室检查进一步明确血小板减少的病因,进行诊断和鉴别诊断(表3)。
表 3 HRT鉴别诊断Table 3. Differential diagnosis of HRT病因 疾病 临床特征 实验室/影像检查 血小板生成减少 AA[16] 全血细胞减少,网织红细胞计数减少,淋巴细胞比例增高;多部位骨髓增生减低或重度减低;小粒空虚,非造血细胞比例增高;巨核细胞明显减少或缺如;红系、粒系细胞均明显减少;骨髓活检全切片增生减低,造血组织减少,非造血细胞增多,网硬蛋白不增加,无异常细胞 血常规、骨髓穿刺、骨髓活检、TPO水平检测、血小板抗体检测、TEG 肿瘤骨髓转移[17] 临床症状为骨痛、脊髓压迫、病理性骨折、出血;血液系统改变多见于血细胞减少,包括一系或二系血细胞减少,最常见的是贫血,其次是TP 骨髓涂片、骨髓活检、TPO水平检测、PET-CT、免疫细胞化学、流式细胞仪、分子测定和荧光原位杂交 营养不良 由于摄入的造血物质不足,长期营养不良很有可能会引起巨幼细胞性贫血等症状 维生素B12、叶酸、TPO水平检测 药物诱导的非免疫性TP 发病前应有确切的应用引起血小板减少的药物(化疗、肿瘤靶向、免疫治疗等药物)停药后血小板减少所致症状与体征逐渐减轻或血小板计数恢复正常;再次使用同样抗肿瘤药物后,TP再次出现 血常规、TPO水平检测 血小板破坏增加 感染[18] 因感染性疾病就诊,出血症状较轻或不明显;实验室检查:外周血象WBC水平升高,Hb轻度降低,血小板轻度或中度减少,严重时可降至10×109/L~20×109/L。纤维蛋白原偏高 血常规、骨髓穿刺、血小板抗体检查、C反应蛋白、降钙素原、病原学诊断、TPO水平检测 免疫性TP[12] 至少连续2次血常规检查示血小板计数减少,外周血涂片镜检血细胞形态无明显异常;脾脏一般不增大;巨核细胞增多或正常,伴成熟障碍,幼稚或颗粒型巨核细胞比例明显增多,产血小板型巨核细胞减少或缺如 血常规、血涂片、骨髓活检、血小板抗体检测、影像学检查、TPO浓度检测、TEG 风湿免疫系统疾病[19]:系统性红斑狼疮、干燥综合征、类风湿关节炎、成人斯蒂尔病等 部分患者并发血小板减少,且疾病不同可伴有不同程度出血现象,包括皮肤、黏膜、消化道出血等症状。骨髓绝大多数无异常,巨核细胞成熟无障碍,产板无减少 血常规、抗核抗体、类风湿因子、TPO水平检测、血小板抗体检测 妊娠期血小板减少[20] 妊娠前及既往无血小板减少病史,多见于妊娠中晚期,期间无其他相关临床表现及出血史;患者虽有血小板下降,但MPV、PDW并无变化 血清铁蛋白、叶酸、维生素B12水平、TEG 血小板分布异常 脾功能亢进 存在脾肿大和全血细胞减少,骨髓巨核细胞功能未受损,形态无异常改变 血常规、B超、MRI等辅助检查、TPO水平检测 血小板消耗增加 药源性血小板减少症(DITP) 用药(抗生素、肝素等)后出现血小板减少,停药后血小板计数恢复;重新用药后血小板再次减少 血常规、抗核抗体、HIT抗体检测、TEG、TPO水平检测 溶血性贫血[21]、阵发性睡眠血红蛋白尿 慢性溶血多表现贫血、黄疸和脾肿大三大特征,可并发胆石症和肝功能损害。急性溶血发病急骤,短期大量溶血引起寒战、发热、头痛、呕吐、四肢腰背疼痛及腹痛,继之出现血红蛋白尿,严重者可发生急性肾衰竭、周围循环衰竭或休克,其后出现黄疸、面色苍白和其他严重贫血的症状和体征 血常规、骨髓涂片、抗人球蛋白试验、蔗糖溶血试验、流式细胞术检测、酸化血清溶血试验等进行溶血筛查 弥漫性血管内凝血[22] 有多部位的出血倾向,皮肤瘀斑、紫癜、咯血、消化道出血等症状 凝血酶原时间、部分活化凝血酶原时间、凝血酶时间、纤维蛋白原、D-二聚体、纤维蛋白降解产物、TPO水平检测、血小板抗体检测 其他 EDTA相关假性TP[23] 患者并无血小板减少,减少的表象是因为血小板与抗凝剂在体外反应而聚集于抗凝管中;通过新鲜样本或检查外周血涂片重复血小板计数检查 血常规、荧光染色法(P-LT-O法)复检 推荐意见4:根据病史、实验室化验、影像学检查结合血小板功能检测指标对HRT和/或其他相关性疾病进行鉴别诊断(推荐级别:2B)。
4.3 TP分级
TP最常用的严重程度分级标准参考美国国家癌症研究所的不良事件术语标准(CTCAE)。根据CTCAE(v.5.0)不良事件“血小板减少症”分级[24](表4)。
表 4 TP分级标准Table 4. Criteria for grading thrombocytopenia级别 血小板计数(×109/L) 1级 ≥75~<100 2级 ≥50~<75 3级 ≥25~<50 4级 <25 通常当患者血小板计数>50×109/L时,出血症状较少见;血小板计数(25~50)×109/L时,患者可表现为皮肤紫癜、瘀斑;血小板计数(10~25)×109/L时,患者会因外伤出血难止;血小板计数<10×109/L时,患者可能出现危及生命的出血风险。
推荐意见5:根据患者血小板计数判定临床TP的严重等级,评估出血风险,给予相应治疗,预防出血的发生(推荐级别:2B)。
5. 治疗
5.1 治疗目标及时机
TP管理的主要目的是预防和治疗出血,避免延迟或影响相关治疗。血小板计数≥50×109/L是临床及文献报道中常见的干预目标值,但血小板计数的安全阈值往往因实施手术或操作者的技术水平、手术或操作本身的出血风险和患者自身其他出凝血情况而异[25]。肝病患者血小板减少同时往往伴随凝血功能异常,如凝血酶原时间、活化部分凝血酶原时间、凝血酶时间显著延长,凝血酶原活动度、纤维蛋白原下降,D-二聚体值增加等,其中凝血酶原活动度<30%的重症肝病患者经外周静脉穿刺中心静脉置管(peripherally inserted central venous catheter,PICC)局部渗血率高达100%。肝病患者处于出血再平衡状态,促凝和抗凝因子同时下降,以下推荐的血小板计数参考阈值仅为相对禁忌(表5)。
表 5 HRT患者诊疗相关操作血小板计数参考阈值推荐Table 5. Recommendation of reference threshold for platelet count in diagnosis and treatment related procedures of patients with HRT诊疗类型 血小板计数参考阈值 操作或手术 胸穿、腹穿;内镜检查;中心静脉置管[25] ≥20×109/L 拔牙[26] ≥40×109/L 腰椎穿刺[25];内镜下活检、食管胃底静脉曲张镜下治疗、大息肉切除,内镜下治疗出血,内镜下逆行胰胆管造影括约肌切开术,或内镜下超声细针穿刺[25];经皮肝穿[27];TACE[28];消融[29];HAIC[30];TIPS[31];PTCD;非神经手术[25];人工肝血液净化治疗[32] ≥50×109/L 神经或血管手术[26] ≥100×109/L 系统治疗 免疫治疗(PD-1/PD-L1)[33] ≥50×109/L 靶向治疗(酪氨酸激酶抑制剂)[34] ≥60×109/L 化疗[35] ≥75×109/L 其他 钇-90(90Y)微球选择性内放射治疗[36] ≥80×109/L 注:PTCD,经皮肝内胆道引流术;TIPS,经颈静脉肝内门体分流术。 推荐意见6:对于接受侵入性操作、手术及抗肿瘤药物治疗的HRT患者,建议参考上述血小板阈值,必要时给予升血小板治疗,以确保治疗的相对安全(推荐级别:2B)。对于肝病合并TP患者,消化内镜诊治前,需充分告知潜在的出血风险。有条件者,建议通过输注血小板等方法,将血小板提升至50×109/L以上,以降低出血风险(推荐级别:2B)。
推荐意见7:HRT的病理生理机制复杂,往往非单一病因所致,且同一病因往往可通过不同病理生理机制引发血小板减少。因此,具体治疗方案的选择需在病因治疗基础上,根据TP的病因、病理生理机制和患者的风险获益综合决策,避免非必要的升血小板治疗(推荐级别:2B)。
5.2 促血小板生成类药物
5.2.1 血小板生成素受体激动剂(TPO receptor agonist,TPO-RA)
目前,国内已获批上市的TPO-RA包括罗普司亭、阿伐曲泊帕、芦曲泊帕、艾曲泊帕和海曲泊帕,其中阿伐曲泊帕和芦曲泊帕获批用于HRT。
阿伐曲泊帕两项Ⅲ期研究显示,择期行侵入性操作的肝病合并TP(血小板<50×109/L)患者,治疗组无需血小板输注或发生出血需抢救的患者比例均显著高于安慰剂组,且侵入性操作当天血小板计数≥50×109/L患者比例更高、血小板计数增幅更大[37]。一项肝癌回顾性研究[38]显示,合并重度TP(血小板<50×109/L)的患者,给予阿伐曲泊帕连续治疗5 d,81.7%患者血小板计数峰值≥50×109/L且相较基线增幅≥20×109/L,对阿伐曲泊帕应答患者肿瘤的疾病控制率较高。此外,有报道阿伐曲泊帕用于重型肝炎相关AA和仑伐替尼相关SAA患者的造血功能改善明显[39-40]。
芦曲泊帕通过日本(L-PLUS1)、全球(L-PLUS2)和中国的Ⅲ期研究[41-42]证实了其疗效和安全性确切,可有效降低血小板输注和急救性输血风险。此外,芦曲泊帕是TPO-RA类目前唯一无饮食限制的口服药物[43],主要经CYP4A11酶进行代谢,与常规药物互不影响。
研究报道相比安慰剂对照组,艾曲泊帕能够显著降低患者操作前至操作后7天血小板输注的比例(72% vs 19%,P<0.001)[44],但有发生急性肝衰的风险[45],FDA和NMPA均给予艾曲泊帕肝毒性的黑框警告。
罗普司亭小样本研究[46]提示术前用于HCV感染相关TP患者(血小板<50×109/L),可使大部分患者血小板≥70×109/L。海曲泊帕至今未见HRT的临床研究报道。
5.2.2 重组人血小板生成素(recombinant human thrombopoietin,rhTPO)
rhTPO与内源性血小板生成素具有相似的升高血小板的药理作用,可针对肝病患者TPO生成减少发挥外源性补充作用,目前正在开展治疗拟择期行侵入性手术的慢性肝病相关血小板减少症患者的Ⅲ期注册临床研究。已有研究[47-48]显示rhTPO用于治疗肝病相关血小板减少症可显著提升血小板计数,减少出血风险及降低血小板输注率。病毒性肝炎肝硬化合并血小板<30×109/L的患者,rhTPO治疗后1个月、6个月时血小板提升到基线2倍的比例最高能达到73.3%和54.8%[47];慢性肝病血小板<50×109/L的患者rhTPO治疗后血小板计数平均增加(58.65±79.24)×109/L,90%患者无需输注血小板[48]。
5.2.3 重组人白介素-11(recombinant human interleukin-11,rhIL-11)
rhIL-11在中国获批用于实体瘤、非髓性白血病化疗后3~4级TP的治疗。肝硬化脾功能亢进所致TP(血小板计数≤75×109/L)患者接受皮下注射rhIL-11 3 mg/次,1次/d,平均治疗时间(6.82±3.51)天,治疗结束后血小板计数平均升高幅度仅为(5.95±12.31)×109/L[49]。此外,rhIL-11球结膜充血、心动过速、水钠潴留等副作用发生率较高,用药时需观察是否会加重患者腹水症状(表6、7)。
Table 6. Thrombopoietic agents approved for market in China (NMPA)项目 rhIL-11 rhTPO 罗普司亭 艾曲泊帕 阿伐曲泊帕 芦曲泊帕 海曲泊帕 TPO受体结合 NA 胞外 胞外 跨膜,胞外 跨膜 跨膜 跨膜 给药途径 注射 注射 注射 口服 口服 口服 口服 半衰期 (6.9±1.7) h (40.2±9.4) h 1~34 d(中位3.5 d) 21~32 h 约为19 h 约为27 h 11.9~40.1 h 饮食影响 NA NA NA 是 是 否 是 与阳离子相互作用 无 无 无 ++ 无 无 ++ 肝功能不全者需降低剂量 否 否 否 是 否 否 是 需增加肝功能监测 否 否 否 是 否 否 是 可用于肾衰竭 需减量 是 是 可能可以 可能可以 可能可以 无数据 国内获批适应证 CIT CIT、ITP二线 ITP二线 ITP二线 择期行诊断性操作或者手术的慢性HRT的成年患者 计划接受手术(含诊断性操作)的慢性肝病伴TP的成年患者 ITP二线、SAA二线 注:CIT,肿瘤化疗相关血小板减少症。 表 7 促血小板生成类药物用于HRT用法用量推荐Table 7. Recommended usage and dosage of thrombopoietic agents for HRT促血小板生成药物 临床研究数据 备注 本共识推荐用法 研究类型 患者人群及病例数 用法用量 阿伐曲泊帕[37] Ⅲ期 择期行侵入性操作的慢性HRT(血小板<50×109/L)患者(n=277) 血小板<40×109/L,口服阿伐曲泊帕60 mg/d,连续5 d; 血小板40~<50×109/L口服阿伐曲泊帕40 mg/d,连续5 d 血小板<40×109/L,口服阿伐曲泊帕60 mg/d,连续5 d; 血小板40~<50×109/L口服阿伐曲泊帕40 mg/d,连续5 d 芦曲泊帕[41] Ⅲ期 计划接受手术(含诊断性操作)的慢性肝病伴TP(血小板<50×109/L)的成年患者(n=96) 口服芦曲泊帕3 mg/d,连续7 d 口服芦曲泊帕3 mg/d,连续7 d 艾曲泊帕[44] Ⅲ期 择期行侵入性操作的慢性HRT(血小板<50×109/L)患者(n=143) 口服艾曲泊帕75 mg/d,连续14 d Ⅲ期研究因发生6例门静脉血栓导致研究提前终止 因国外血栓风险而暂停Ⅲ期研究,所以待积累国内临床用药经验后再补充 罗普司亭[46] 单中心、单臂、开放标签 择期手术的HCV感染继发血小板减少(血小板<50×109/L)患者(n=35) 注射罗普司亭2 μg/kg,1次/周,最长给药1个月,目标血小板为70×109/L 2 μg/kg皮下注射,1次/周,1~2周 停药标准:连续两次血小板≥70×109/L rhTPO[47-48] 多中心、真实世界研究 乙型肝炎肝硬化合并TP(血小板<30×109/L)(单药组,n=29) rhTPO 15 000U皮下注射,1次/d,治疗中位时间4周 15 000U皮下注射,1次/d,7 d 停药标准:当血小板计数升高至≥50×109/L且较基线升高≥10×109/L 单中心、单臂、回顾性分析 择期行侵入性操作肝病合并TP(血小板<50×109/L)患者(n=100) rhTPO 15 000U皮下注射,1次/d,平均用药12 d rhIL-11[49] 单中心、非随机对照研究 肝硬化脾功能亢进所致TP(血小板<75×109/L)患者(n=42) 皮下注射rhIL-11 3 mg/次,1次/d,平均治疗时间(6.82±3.51)d 说明书提到水钠潴留副作用 皮下注射,3 mg/次,1次/d,连续7~14 d 推荐意见8:拟接受择期操作、手术或特殊治疗的HRT患者,术前可给予促血小板生成类药物治疗以达到要求的血小板计数阈值,但需监测血小板计数,以免增加血栓形成风险(推荐级别:2A)。
5.3 免疫抑制剂
有研究[52]报道慢性肝病合并ITP患者进行糖皮质激素治疗可达到完全缓解或部分缓解。HBV感染可能是诱发ITP的病毒之一,但是糖皮质激素等免疫抑制剂治疗可能导致HBV再激活,严重者可发生肝衰竭。因此,HBV感染者合并继发免疫性血小板减少症应用糖皮质激素等免疫抑制剂治疗时,应同时应用恩替卡韦、富马酸替诺福韦二吡呋酯或富马酸丙酚替诺福韦进行抗病毒治疗(表8)。
表 8 糖皮质激素用法用量参考Table 8. Usage and dosage of glucocorticoid for reference激素用量(mg/d) 减量方法 60 血小板≥30×109/L后减量 30~40 持续1周 20 持续1周 10 持续1周 5 维持 注:依据病情酌情调整。 推荐意见9:糖皮质激素等免疫抑制剂治疗HBV感染患者合并继发免疫性TP时应同时应用恩替卡韦、富马酸替诺福韦二吡呋酯或富马酸丙酚替诺福韦进行抗病毒治疗,以防HBV再激活(推荐级别:2A)。
5.4 有创治疗
肝病患者继发脾肿大/脾功能亢进相关TP的有创治疗措施包括脾脏切除、部分脾动脉栓塞(partial splenic embolization,PSE)、热消融等。有创治疗可使脾肿大/脾功能亢进相关TP患者获得相对长期的持续改善,但PSE和热消融治疗后血小板持续改善时间往往与脾栓或消融的体积密切相关,且往往面临较高的术后并发症发生风险,远期获益仍待进一步评估。
5.4.1 部分脾动脉栓塞(PSE)
PSE可提升并维持较长时间的血小板计数,但栓塞面积较难掌握,术后易出现间歇性发热、腹痛、恶心、呕吐、腹胀、食欲不振和栓塞后综合征,且肝硬化患者脾动脉栓塞有较高的内脏静脉血栓形成风险,术后内脏静脉血栓的发生率达11.7%[53]。肝硬化并发门静脉高压症患者接受TIPS联合PSE治疗后血小板计数获显著提升,术后7天较术前血小板提升200×109/L左右,早期给予低分子肝素联合华法林抗凝处理能有效预防TIPS联合PSE术后门静脉系统血栓形成,门静脉血栓形成发生率为2.3%[54]。
5.4.2 脾脏热消融治疗
热消融用于治疗门静脉高压性脾功能亢进具有微创、安全、疗效显著等优点,其理想的消融量为50%~70%。但热消融因目前没有统一应用标准、对操作者的技术要求较高、射频仪器及耗材费用高等原因,实际应用较少。研究[55]报道肝硬化脾功能亢进患者分别接受热消融和脾切除治疗,随访36个月时RFA组外周血小板计数显著降低,48个月时恢复至基线水平,其中脾消融率低于50%患者脾功能亢进在6个月后复发。
5.4.3 脾脏切除术
有报道[56]肝细胞癌(HCC)合并肝硬化患者脾切除术后血小板计数获得3年持续改善。术后门静脉或脾静脉血栓,胰腺损伤发生率更高,但围手术期死亡率相比未行脾切患者无明显增加;静脉曲张再出血、肿瘤进展或复发明显降低,但长期死亡率无显著差异[57]。此外,研究提示肝硬化合并门静脉高压和脾功能亢进患者接受脾次全切除术可长期改善食管胃底静脉曲张破裂出血[58],但肝硬化患者在脾切除术后门静脉或脾静脉血栓形成事件发生率可达22.2%[59]。
推荐意见10:脾脏切除术、脾脏栓塞术、脾脏热消融术等有创治疗用于HRT患者需充分评估患者的风险与获益,建议术前采取MDT模式,综合各学科意见,制定最佳治疗方案,并注意术后血栓等并发症的防治(推荐级别:2B)。
5.5 血小板输注
一个单位的浓缩血小板(标准成人血小板剂量)含(300±33)×109个血小板,血小板浓缩物储存温度为20 ℃~24 ℃,持续轻缓振摇不超过5 d[60]。研究发现肝硬化合并血小板减少患者输注1个标准成人剂量血小板后,血小板计数中位数可从39×109/L(16×109/L~64×109/L)提升至52×109/L(19×109/L~91×109/L)[61];肝病患者术前输注2 U血小板术后24 h血小板变化值为(15.17±18.23)×109/L,输注1 U血小板变化值为(9.02±11.25)×109/L[61];慢性肝病患者通过血小板输注将血小板计数提升至50×109/L以上仅能维持2 d[62]。
部分血小板减少患者在连续2次及以上接受足够剂量血小板输注后,会出现临床出血症状未见改善、血小板计数未见明显增高等血小板输注无效(platelet transfusion refractoriness,PTR)情况,而输注经配型选择的相容性血小板是解决免疫性因素所致PTR的有效方法。反复血小板输注的相关风险有:(1)产生同种免疫,使以后的血小板输注疗效降低,是多次输注患者常见问题。(2)不良反应:以非溶血性发热和过敏反应多见,报告发生率为3%[63]。
推荐意见11:血小板输注仍是最快提升血小板计数的治疗措施,可用于各种病因及病理生理机制所致血小板减少;鉴于其保存期短、临床供应紧缺及潜在输注风险等,建议仅用于有危及生命出血风险及需接受紧急手术患者(推荐级别:2B)。
推荐意见12:导致血小板输注无效的原因通常有非免疫性因素和免疫性因素;针对非免疫性因素进行对症治疗或者排除病因,对明确诊断免疫性血小板输注无效患者,应申请血小板配型(推荐级别:2A)。
5.6 其他治疗
利可君、咖啡酸片等在临床实践中常被用于各种原因所致TP,小样本研究提示利可君、咖啡酸片亦可一定程度改善HRT患者血小板计数。此外,中医学基于整体观念进行辨证论治,TP多从虚证辨治,如阴虚血热则滋阴退热,气血亏虚则益气养血,再佐以止血类中药预防出血,在改善患者全身症状的同时,对HRT具有一定临床疗效。研究[64]也提示在肝癌的治疗方案中联合中药辨证论治,可降低治疗相关的TP的发生率。
推荐意见13:HRT患者根据血小板减少的严重程度及紧急性,在血小板输注、应用升血小板药物等治疗基础上,经中医辨证后可联合中医中药治疗(推荐级别:2B)。
6. HRT患者的抗凝治疗
肝硬化患者门静脉血栓(portal vein thrombosis,PVT)患病率为5%~20%,年发病率为3%~17%[65]。有2项Meta分析研究提示,抗凝治疗后肝硬化PVT的门静脉再通率为66%~71%,门静脉完全再通率为41.5%~53%[66-67]。一项随机对照研究[68]发现,低分子肝素注射治疗1个月后口服华法林5个月的抗凝治疗方案对肝硬化PVT患者安全、有效。显然抗凝治疗对肝硬化患者PVT具有很好的治疗效果,但临床上仍然担心抗凝治疗可能带来的出血风险,尤其是肝硬化失代偿期患者;《肝硬化门静脉血栓管理专家共识》将近期出血史、严重的胃底食管静脉曲张、严重的TP作为肝硬化患者抗凝治疗的主要禁忌证[69]。国际静脉血栓栓塞医学预防登记处(PROVEE)的数据来评估住院患者出血发生率,发现血小板计数<50×109/L、肝衰竭、既往有出血史和胃十二指肠溃疡是住院患者发生出血的危险因素且可能会影响抗凝治疗[70];另有研究表明,当血小板计数<50×109/L时,癌症患者接受静脉血栓栓塞症的抗凝治疗出血风险显著增加[71]。针对慢性肝病血小板减少症患者应该选择何种的抗凝方案才能减少出血风险,相关支持性研究较少。“2022 EHA指南:肿瘤合并TP患者抗栓治疗管理”[72]推荐3级TP伴静脉血栓栓塞或房颤患者不使用口服抗凝剂和维生素K拮抗剂;平衡出血和血栓形成风险后,急性静脉血栓栓塞患者应使用低分子肝素,预防性或治疗性剂量均应减少50%。4级TP患者不推荐进行抗凝治疗。
推荐意见14:肝病合并血小板计数<50×109/L的患者,抗凝治疗需充分评估出血和血栓风险后谨慎进行,低分子肝素剂量需减半或暂缓治疗(推荐级别:2B)。
7. 总结和展望
本共识汇总了HRT领域的最新文献、临床研究报道、相关指南或共识,综合了共识编撰专家的临床经验及意见,推荐意见考虑了目前HRT治疗措施提升血小板计数的有效性及其潜在不良反应,方案实施时需结合患者的具体情况,充分评估患者的出血及血栓风险,平衡风险获益,为广大临床医生提供了HRT诊断、鉴别诊断及临床治疗管理的全方位指导(图2)。但本共识所引用的文献多数仍为回顾性或前瞻性观察性研究,患者接受侵入性操作或手术的血小板安全阈值、脾切除等有创治疗的获益人群、血栓合并重度TP的抗凝治疗等临床问题仍缺乏高水平的循证医学证据。后续随着该领域循证的不断积累,本共识将依据新的临床证据进行相应调整和修订。
共识编撰委员会
主任委员:王福生(解放军总医院第五医学中心)
副主任委员:陆荫英(解放军总医院第五医学中心)、刘连新(中国科学技术大学附属第一医院)、胡亮钉(解放军总医院第五医学中心)、高春记(解放军总医院第五医学中心)、虞朝辉(浙江大学医学院附属第一医院)、张晶(首都医科大学附属北京佑安医院)
执笔:于航(解放军总医院第五医学中心)、闫涛(解放军总医院第五医学中心)、孙耀(解放军总医院第五医学中心) 委员会专家(按姓氏拼音排序):安勇(山东第一医科大学第一附属医院)、陈荣新(复旦大学附属中山医院)、陈韬(华中科技大学同济医学院附属同济医院)、程家敏(解放军总医院第五医学中心)、党双锁(西安交通大学第二附属医院)、董政(解放军总医院第五医学中心)、高春记(解放军总医院第五医学中心)、高沿航(吉林大学白求恩第一医院)、郜玉峰(安徽医科大学第一附属医院)、胡亮钉(解放军总医院第五医学中心)、黄建荣(浙江大学医学院附属第一医院)、金龙(首都医科大学附属北京友谊医院)、黎军和(南昌大学第一附属医院)、陆伟(上海市公共卫生临床中心)、陆荫英(解放军总医院第五医学中心)、卢实春(解放军总医院第一医学中心)、路筝(解放军总医院第五医学中心)、李海洋(贵州医科大学附属医院)、李建军(首都医科大学附属北京佑安医院)、李克(厦门大学附属翔安医院)、李卫(阜阳市第二人民医院)、李文华(太原市第三人民医院)、李志伟(深圳市第三人民医院)、郭亚兵(南方医科大学南方医院)、郭亚荣(山西医科大学第一医院)、高杰(北京大学人民医院)、刘连新(中国科学技术大学附属第一医院)、刘传苗(蚌埠医学院第一附属医院)、刘振洋(湖南省肿瘤医院)、孟繁平(解放军总医院第五医学中心)、南月敏(河北医科大学第三医院)、牛作兴(山东省肿瘤医院)、宁红梅(解放军总医院第五医学中心)、宁琴(华中科技大学同济医学院附属同济医院)、彭涛(广西医科大学第一附属医院)、彭仕芳(中南大学湘雅医院)、曲秀娟(中国医科大学附属第一医院)、宋天强(天津市肿瘤医院)、孙剑(南方医科大学南方医院)、孙耀(解放军总医院第五医学中心)、沈洁(南京大学医学院附属鼓楼医院)、唐红(四川大学华西医院)、汪海涛(解放军总医院第四医学中心)、王晗(解放军总医院第五医学中心)、王军(解放军总医院第五医学中心)、王继洲(中国科学技术大学附属第一医院)、王帅(解放军总医院第五医学中心)、王文涛(四川大学华西医院)、王维虎(北京大学肿瘤医院)、王祥耀(解放军总医院第一医学中心)、王辛(四川大学华西医院)、吴建兵(南昌大学第二附属医院)、夏峰(重庆西南医院)、夏勇(海军军医大学东方肝胆外科医院)、夏志波(空军特色医学中心)、谢青(上海交通大学医学院附属瑞金医院)、徐磊(解放军总医院第五医学中心)、闫涛(解放军总医院第五医学中心)、杨永峰(南京市第二医院)、于航(解放军总医院第五医学中心)、虞朝辉(浙江大学医学院附属第一医院)、余灵祥(解放军总医院第五医学中心)、余祖江(郑州大学第一附属医院)、应杰儿(浙江省肿瘤医院)、袁振刚(海军军医大学东方肝胆外科医院)、曾珊(中南大学湘雅医院)、曾扬(解放军总医院第五医学中心)、张晶(首都医科大学附属北京佑安医院)、张岚(复旦大学附属中山医院)、赵海涛(北京协和医院)、赵明(中山大学附属肿瘤医院)、赵雪珂(贵州医科大学附属医院)、赵新颖(首都医科大学附属北京友谊医院)、左石(贵州医科大学附属医院)
-
表 1 推荐级别及定义
Table 1. Recommendation grades and definitions
推荐级别 代表意义 1类 基于高级别临床证据,专家意见高度一致 2A类 基于低级别临床证据,专家意见高度一致;或基于高级别证据,专家意见基本一致 2B类 基于低级别临床证据,专家意见基本一致 3类 不论基于何种级别临床证据,专家意见明显分歧 表 2 血小板功能相关检测
Table 2. Platelet function related tests
指标 检测设备 标本 正常值 临床意义 TPO水平检测 离心机、37 ℃恒温水浴箱、酶标仪、移液器、洗板机等 血清样本或血浆(EDTA或柠檬酸钠或肝素抗凝)样本均可 最广泛使用的ELISA法测定的正常值为(64±41)pg/mL(范围27~188 pg/mL) 根据《成人原发免疫性血小板减少症诊断与治疗中国指南(2020年版)》,血清TPO水平测定的意义:(1)鉴别不典型再生障碍性贫血(AA)、低增生骨髓增生异常综合征;(2)用于常规治疗无效患者及脾切除前疾病重新评估 TEG TEG仪(检测方法按仪器说明书进行操作) 动脉血或静脉血均可 参考医院提供的实验室检查正常值范围标准 凝血因子定性分析、纤维蛋白原的定性分析、血小板数量与质量的定性分析、检测血液中是否有肝素的影响、测定纤溶活性、诊断高凝状态、判断血栓风险、鉴别术后渗血和出血、准确判断原因、诊断弥散性血管内凝血(DIC)、监测体外循环和心脏介入治疗等的抗凝情况、监测肝移植手术的出血及凝血状态,以及监测抗血小板药物治疗效果和并发症等 血小板抗体检查 离心机、恒温水浴箱、酶标仪、移液器、振荡器等 血清样本或血浆(EDTA或枸橼酸钠抗凝)样本均可 结果判定:阴性 用途:(1)人类血小板抗原(HPA)抗体检测;(2)HPA型。 根据《成人原发免疫性血小板减少症诊断与治疗中国指南(2020年版)》,血小板糖蛋白特异性自身抗体检查的意义:(1)鉴别非免疫性血小板减少;(2)常规治疗无效患者及脾切除前疾病重新评估;(3)指导静脉注射人免疫球蛋白治疗 注:EDTA,乙二胺四乙酸。 表 3 HRT鉴别诊断
Table 3. Differential diagnosis of HRT
病因 疾病 临床特征 实验室/影像检查 血小板生成减少 AA[16] 全血细胞减少,网织红细胞计数减少,淋巴细胞比例增高;多部位骨髓增生减低或重度减低;小粒空虚,非造血细胞比例增高;巨核细胞明显减少或缺如;红系、粒系细胞均明显减少;骨髓活检全切片增生减低,造血组织减少,非造血细胞增多,网硬蛋白不增加,无异常细胞 血常规、骨髓穿刺、骨髓活检、TPO水平检测、血小板抗体检测、TEG 肿瘤骨髓转移[17] 临床症状为骨痛、脊髓压迫、病理性骨折、出血;血液系统改变多见于血细胞减少,包括一系或二系血细胞减少,最常见的是贫血,其次是TP 骨髓涂片、骨髓活检、TPO水平检测、PET-CT、免疫细胞化学、流式细胞仪、分子测定和荧光原位杂交 营养不良 由于摄入的造血物质不足,长期营养不良很有可能会引起巨幼细胞性贫血等症状 维生素B12、叶酸、TPO水平检测 药物诱导的非免疫性TP 发病前应有确切的应用引起血小板减少的药物(化疗、肿瘤靶向、免疫治疗等药物)停药后血小板减少所致症状与体征逐渐减轻或血小板计数恢复正常;再次使用同样抗肿瘤药物后,TP再次出现 血常规、TPO水平检测 血小板破坏增加 感染[18] 因感染性疾病就诊,出血症状较轻或不明显;实验室检查:外周血象WBC水平升高,Hb轻度降低,血小板轻度或中度减少,严重时可降至10×109/L~20×109/L。纤维蛋白原偏高 血常规、骨髓穿刺、血小板抗体检查、C反应蛋白、降钙素原、病原学诊断、TPO水平检测 免疫性TP[12] 至少连续2次血常规检查示血小板计数减少,外周血涂片镜检血细胞形态无明显异常;脾脏一般不增大;巨核细胞增多或正常,伴成熟障碍,幼稚或颗粒型巨核细胞比例明显增多,产血小板型巨核细胞减少或缺如 血常规、血涂片、骨髓活检、血小板抗体检测、影像学检查、TPO浓度检测、TEG 风湿免疫系统疾病[19]:系统性红斑狼疮、干燥综合征、类风湿关节炎、成人斯蒂尔病等 部分患者并发血小板减少,且疾病不同可伴有不同程度出血现象,包括皮肤、黏膜、消化道出血等症状。骨髓绝大多数无异常,巨核细胞成熟无障碍,产板无减少 血常规、抗核抗体、类风湿因子、TPO水平检测、血小板抗体检测 妊娠期血小板减少[20] 妊娠前及既往无血小板减少病史,多见于妊娠中晚期,期间无其他相关临床表现及出血史;患者虽有血小板下降,但MPV、PDW并无变化 血清铁蛋白、叶酸、维生素B12水平、TEG 血小板分布异常 脾功能亢进 存在脾肿大和全血细胞减少,骨髓巨核细胞功能未受损,形态无异常改变 血常规、B超、MRI等辅助检查、TPO水平检测 血小板消耗增加 药源性血小板减少症(DITP) 用药(抗生素、肝素等)后出现血小板减少,停药后血小板计数恢复;重新用药后血小板再次减少 血常规、抗核抗体、HIT抗体检测、TEG、TPO水平检测 溶血性贫血[21]、阵发性睡眠血红蛋白尿 慢性溶血多表现贫血、黄疸和脾肿大三大特征,可并发胆石症和肝功能损害。急性溶血发病急骤,短期大量溶血引起寒战、发热、头痛、呕吐、四肢腰背疼痛及腹痛,继之出现血红蛋白尿,严重者可发生急性肾衰竭、周围循环衰竭或休克,其后出现黄疸、面色苍白和其他严重贫血的症状和体征 血常规、骨髓涂片、抗人球蛋白试验、蔗糖溶血试验、流式细胞术检测、酸化血清溶血试验等进行溶血筛查 弥漫性血管内凝血[22] 有多部位的出血倾向,皮肤瘀斑、紫癜、咯血、消化道出血等症状 凝血酶原时间、部分活化凝血酶原时间、凝血酶时间、纤维蛋白原、D-二聚体、纤维蛋白降解产物、TPO水平检测、血小板抗体检测 其他 EDTA相关假性TP[23] 患者并无血小板减少,减少的表象是因为血小板与抗凝剂在体外反应而聚集于抗凝管中;通过新鲜样本或检查外周血涂片重复血小板计数检查 血常规、荧光染色法(P-LT-O法)复检 表 4 TP分级标准
Table 4. Criteria for grading thrombocytopenia
级别 血小板计数(×109/L) 1级 ≥75~<100 2级 ≥50~<75 3级 ≥25~<50 4级 <25 表 5 HRT患者诊疗相关操作血小板计数参考阈值推荐
Table 5. Recommendation of reference threshold for platelet count in diagnosis and treatment related procedures of patients with HRT
诊疗类型 血小板计数参考阈值 操作或手术 胸穿、腹穿;内镜检查;中心静脉置管[25] ≥20×109/L 拔牙[26] ≥40×109/L 腰椎穿刺[25];内镜下活检、食管胃底静脉曲张镜下治疗、大息肉切除,内镜下治疗出血,内镜下逆行胰胆管造影括约肌切开术,或内镜下超声细针穿刺[25];经皮肝穿[27];TACE[28];消融[29];HAIC[30];TIPS[31];PTCD;非神经手术[25];人工肝血液净化治疗[32] ≥50×109/L 神经或血管手术[26] ≥100×109/L 系统治疗 免疫治疗(PD-1/PD-L1)[33] ≥50×109/L 靶向治疗(酪氨酸激酶抑制剂)[34] ≥60×109/L 化疗[35] ≥75×109/L 其他 钇-90(90Y)微球选择性内放射治疗[36] ≥80×109/L 注:PTCD,经皮肝内胆道引流术;TIPS,经颈静脉肝内门体分流术。 表 6 中国(NMPA)获批上市的促血小板生成类药物[50-51]
Table 6. Thrombopoietic agents approved for market in China (NMPA)
项目 rhIL-11 rhTPO 罗普司亭 艾曲泊帕 阿伐曲泊帕 芦曲泊帕 海曲泊帕 TPO受体结合 NA 胞外 胞外 跨膜,胞外 跨膜 跨膜 跨膜 给药途径 注射 注射 注射 口服 口服 口服 口服 半衰期 (6.9±1.7) h (40.2±9.4) h 1~34 d(中位3.5 d) 21~32 h 约为19 h 约为27 h 11.9~40.1 h 饮食影响 NA NA NA 是 是 否 是 与阳离子相互作用 无 无 无 ++ 无 无 ++ 肝功能不全者需降低剂量 否 否 否 是 否 否 是 需增加肝功能监测 否 否 否 是 否 否 是 可用于肾衰竭 需减量 是 是 可能可以 可能可以 可能可以 无数据 国内获批适应证 CIT CIT、ITP二线 ITP二线 ITP二线 择期行诊断性操作或者手术的慢性HRT的成年患者 计划接受手术(含诊断性操作)的慢性肝病伴TP的成年患者 ITP二线、SAA二线 注:CIT,肿瘤化疗相关血小板减少症。 表 7 促血小板生成类药物用于HRT用法用量推荐
Table 7. Recommended usage and dosage of thrombopoietic agents for HRT
促血小板生成药物 临床研究数据 备注 本共识推荐用法 研究类型 患者人群及病例数 用法用量 阿伐曲泊帕[37] Ⅲ期 择期行侵入性操作的慢性HRT(血小板<50×109/L)患者(n=277) 血小板<40×109/L,口服阿伐曲泊帕60 mg/d,连续5 d; 血小板40~<50×109/L口服阿伐曲泊帕40 mg/d,连续5 d 血小板<40×109/L,口服阿伐曲泊帕60 mg/d,连续5 d; 血小板40~<50×109/L口服阿伐曲泊帕40 mg/d,连续5 d 芦曲泊帕[41] Ⅲ期 计划接受手术(含诊断性操作)的慢性肝病伴TP(血小板<50×109/L)的成年患者(n=96) 口服芦曲泊帕3 mg/d,连续7 d 口服芦曲泊帕3 mg/d,连续7 d 艾曲泊帕[44] Ⅲ期 择期行侵入性操作的慢性HRT(血小板<50×109/L)患者(n=143) 口服艾曲泊帕75 mg/d,连续14 d Ⅲ期研究因发生6例门静脉血栓导致研究提前终止 因国外血栓风险而暂停Ⅲ期研究,所以待积累国内临床用药经验后再补充 罗普司亭[46] 单中心、单臂、开放标签 择期手术的HCV感染继发血小板减少(血小板<50×109/L)患者(n=35) 注射罗普司亭2 μg/kg,1次/周,最长给药1个月,目标血小板为70×109/L 2 μg/kg皮下注射,1次/周,1~2周 停药标准:连续两次血小板≥70×109/L rhTPO[47-48] 多中心、真实世界研究 乙型肝炎肝硬化合并TP(血小板<30×109/L)(单药组,n=29) rhTPO 15 000U皮下注射,1次/d,治疗中位时间4周 15 000U皮下注射,1次/d,7 d 停药标准:当血小板计数升高至≥50×109/L且较基线升高≥10×109/L 单中心、单臂、回顾性分析 择期行侵入性操作肝病合并TP(血小板<50×109/L)患者(n=100) rhTPO 15 000U皮下注射,1次/d,平均用药12 d rhIL-11[49] 单中心、非随机对照研究 肝硬化脾功能亢进所致TP(血小板<75×109/L)患者(n=42) 皮下注射rhIL-11 3 mg/次,1次/d,平均治疗时间(6.82±3.51)d 说明书提到水钠潴留副作用 皮下注射,3 mg/次,1次/d,连续7~14 d 表 8 糖皮质激素用法用量参考
Table 8. Usage and dosage of glucocorticoid for reference
激素用量(mg/d) 减量方法 60 血小板≥30×109/L后减量 30~40 持续1周 20 持续1周 10 持续1周 5 维持 注:依据病情酌情调整。 英文缩写 中文全称 英文缩写 中文全称 AA 再生障碍性贫血 PICC 经外周静脉穿刺中心静脉置管 AIH 自身免疫性肝炎 PLT 血小板 ALD 酒精性肝病 P-LT-O法 荧光染色法 APTT 活化部分凝血酶原时间 PROVEE 国际静脉血栓栓塞医学预防登记处 CIT 肿瘤化疗相关性血小板减少症 PSE 部分脾动脉栓塞 CTCAE 不良事件术语标准 PT 凝血酶原时间 D-D D-二聚体 PTA 凝血酶原活动度 DIC 弥散性血管内凝血 PTCD 经皮肝内胆道引流术 DITP 药源性血小板减少症 PTR 血小板输注无效 DOAC 口服抗凝剂 PVT 门静脉血栓 EDTA 乙二胺四乙酸 RFA 射频消融 FIB 纤维蛋白原 rhIL-11 重组人白介素11 HAIC 肝动脉灌注化疗 rhTPO 重组人血小板生成素 Hb 血红蛋白 SAA 重型再生障碍性贫血 HBV 乙型肝炎病毒 SIRT 选择性体内放射疗法 HCC 肝细胞癌 TACE 经肝动脉化疗栓塞术 HIT 肝素诱导的血小板减少症 TEG 血栓弹力图 HPA 血小板抗原 TIPS 经颈静脉肝内门体分流术 HRT 肝病相关血小板减少症 TP 血小板减少症 ITP 原发免疫性血小板减少症 TPO 血小板生成素 MDT 多学科会诊 TPO-RA 血小板生成素受体激动剂 MPV 平均血小板体积 TT 凝血酶时间 MRI 核磁共振成像 VKAs 维生素K拮抗剂 OS 总生存期 vWF 血管性血友病因子 PDW 血小板分布宽度 WBC 白细胞 PET-CT 正电子发射断层显像 90Y 钇-90 -
[1] GANGIREDDY VGR, KANNEGANTI PC, SRIDHAR S, et al. Management of thrombocytopenia in advanced liver disease[J]. Can J Gastroenterol Hepatol, 2014, 28( 10): 558- 564. DOI: 10.1155/2014/532191. [2] HUANG CH, CHANG JJ, WU YY, et al. Different impacts of common risk factors associated with thrombocytopenia in patients with hepatitis B virus and hepatitis C virus infection[J]. Biomed J, 2022, 45( 5): 788- 797. DOI: 10.1016/j.bj.2021.09.001. [3] LI QJ, HE MK, CHEN HW, et al. Hepatic arterial infusion of oxaliplatin, fluorouracil, and leucovorin versus transarterial chemoembolization for large hepatocellular carcinoma: A randomized phase III trial[J]. J Clin Oncol, 2022, 40( 2): 150- 160. DOI: 10.1200/JCO.21.00608. [4] KUDO M, UESHIMA K, YOKOSUKA O, et al. Sorafenib plus low-dose cisplatin and fluorouracil hepatic arterial infusion chemotherapy versus sorafenib alone in patients with advanced hepatocellular carcinoma(SILIUS): A randomised, open label, phase 3 trial[J]. Lancet Gastroenterol Hepatol, 2018, 3( 6): 424- 432. DOI: 10.1016/S2468-1253(18)30078-5. [5] PECK-RADOSAVLJEVIC M. Thrombocytopenia in chronic liver disease[J]. Liver Int, 2017, 37( 6): 778- 793. DOI: 10.1111/liv.13317. [6] GALLO P, TERRACCIANI F, DI PASQUALE G, et al. Thrombocytopenia in chronic liver disease: Physiopathology and new therapeutic strategies before invasive procedures[J]. World J Gastroenterol, 2022, 28( 30): 4061- 4074. DOI: 10.3748/wjg.v28.i30.4061. [7] ADINOLFI LE, GIORDANO MG, ANDREANA A, et al. Hepatic fibrosis plays a central role in the pathogenesis of thrombocytopenia in patients with chronic viral hepatitis[J]. Br J Haematol, 2001, 113( 3): 590- 595. DOI: 10.1046/j.1365-2141.2001.02824.x. [8] PEREIRA J, ACCATINO L, ALFARO J, et al. Platelet autoantibodies in patients with chronic liver disease[J]. Am J Hematol, 1995, 50( 3): 173- 178. DOI: 10.1002/ajh.2830500305. [9] XIAO H, WANG L. Mechanisms of throm bocytopenia in liver cirrhosis[J]. J Pract Hepatol, 2019, 22( 4): 462- 465. DOI: 10.3969/j.issn.1672-5069.2019.04.003.肖函, 王利. 肝硬化血小板减少的病理生理发生机制[J]. 实用肝脏病杂志, 2019, 22( 4): 462- 465. DOI: 10.3969/j.issn.1672-5069.2019.04.003. [10] MITCHELL O, FELDMAN DM, DIAKOW M, et al. The pathophysiology of thrombocytopenia in chronic liver disease[J]. Hepat Med, 2016, 8: 39- 50. DOI: 10.2147/HMER.S74612. [11] KANEKO J, SUGAWARA Y, MATSUI Y, et al. Normal splenic volume in adults by computed tomography[J]. Hepato-gastroenterology, 2002, 49( 48): 1726- 1727. [12] Thrombosis and Hemostasis Group, Society of Hematology, Chinese Medical Association. Chinese guideline on the diagnosis and management of adult primary immune thrombocytopenia(version 2020)[J]. Chin J Hematol, 2020, 41( 8): 617- 623. DOI: 10.3760/cma.j.issn.0253-2727.2020.08.001中华医学会血液学分会血栓与止血学组, 成人原发免疫性血小板减少症诊断与治疗中国指南(2020年版)[J]. 中华血液学杂志, 2020, 41( 8): 617- 623. DOI: 10.3760/cma.j.issn.0253-2727.2020.08.001 [13] Chinese Society of Hepatology, Chinese Medical Association. Guidelines on the diagnosis and management of autoimmune hepatitis(2021)[J]. J Clin Hepatol, 2022, 38( 1): 42- 49. DOI: 10.3760/cma.j.cn112138-20211112-00796.中华医学会肝病学分会. 自身免疫性肝炎诊断和治疗指南(2021)[J]. 临床肝胆病杂志, 2022, 38( 1): 42- 49. DOI: 10.3760/cma.j.cn112138-20211112-00796. [14] General Office of National Health Commission. Standard for diagnosis and treatment of primary liver cancer(2022 edition)[J]. J Clin Hepatol, 2022, 38( 2): 288- 303. DOI: 10.3969/j.issn.1001-5256.2022.02.009.国家卫生健康委办公厅. 原发性肝癌诊疗指南(2022年版)[J]. 临床肝胆病杂志, 2022, 38( 2): 288- 303. DOI: 10.3969/j.issn.1001-5256.2022.02.009. [15] AL-SAMKARI H, SOFF GA. Clinical challenges and promising therapies for chemotherapy-induced thrombocytopenia[J]. Expert Rev Hematol, 2021, 14( 5): 437- 448. DOI: 10.1080/17474086.2021.1924053. [16] Red Cell Diseases(Anemia) Group, Society of Hematology, Chinese Medical Association. Diagnosis and treatment of aplastic anemia China guide(2022 edition)[J]. Chin J Hematol, 2022( 11): 881- 888.中华医学会血液学分会红细胞疾病(贫血)学组, 再生障碍性贫血诊断与治疗中国指南(2022年版)[J]. 中华血液学杂志, 2022( 11): 881- 888. [17] POCKETT RD, CASTELLANO D, MCEWAN P, et al. The hospital burden of disease associated with bone metastases and skeletal-related events in patients with breast cancer, lung cancer, or prostate cancer in Spain[J]. Eur J Cancer Care, 2010, 19( 6): 755- 760. DOI: 10.1111/j.1365-2354.2009.01135.x. [18] FRANCHINI M, VENERI D, LIPPI G. Thrombocytopenia and infections[J]. Expert Rev Hematol, 2017, 10( 1): 99- 106. DOI: 10.1080/17474086.2017.1271319. [19] KLEIN A, MOLAD Y. Hematological manifestations among patients with rheumatic diseases[J]. Acta Haematol, 2021, 144( 4): 403- 412. DOI: 10.1159/000511759. [20] LI LP, YING H. Etiology and differential diagnosis of thrombocytopenia in pregnancy[J]. Chin J Pract Gynecol Obstet, 2022, 38( 12): 1166- 1170.李莉平, 应豪. 妊娠期血小板减少的原因与鉴别诊断[J]. 中国实用妇科与产科杂志, 2022, 38( 12): 1166- 1170. [21] HE YY. Application value of systematic analysis of hemolytic etiology in diagnosis and differentiation of hereditary hemolytic anemia[J]. Mod Med J China, 2018, 20( 4): 55- 57.何永艳. 溶血病因系统分析在遗传性溶血性贫血诊断和鉴别中的应用价值[J]. 中国现代医药杂志, 2018, 20( 4): 55- 57. [22] IKEZOE T. Advances in the diagnosis and treatment of disseminated intravascular coagulation in haematological malignancies[J]. Int J Hematol, 2021, 113( 1): 34- 44. DOI: 10.1007/s12185-020-02992-w. [23] SALAMA A. Autoimmune thrombocytopenia complicated by EDTA-and/or citrate-dependent pseudothrombocytopenia[J]. Transfus Med Hemother, 2015, 42( 5): 345- 348. DOI: 10.1159/000437220. [24] LI Q, CHEN L, YU XH. Differentiation of bone marrow cell morphology of thrombocytopenia in chronic liver disease and primary immune thrombocytopenia[J]. Chin J Pract Med, 2022, 49( 8): 10- 12. DOI: 10.3760/cma.j.cn115689-20220122-00349.李清, 陈雷, 余晓红. 慢性肝病血小板减少症与原发免疫性血小板减少症的骨髓细胞形态的鉴别[J]. 中国实用医刊, 2022, 49( 8): 10- 12. DOI: 10.3760/cma.j.cn115689-20220122-00349. [25] BIOLATO M, VITALE F, GALASSO T, et al. Minimum platelet count threshold before invasive procedures in cirrhosis: Evolution of the guidelines[J]. World J Gastrointest Surg, 2023, 15( 2): 127- 141. DOI: 10.4240/wjgs.v15.i2.127. [26] ALVARO D, CAPORASO N, GIANNINI EG, et al. Procedure-related bleeding risk in patients with cirrhosis and severe thrombocytopenia[J]. Eur J Clin Invest, 2021, 51( 6): e13508. DOI: 10.1111/eci.13508. [27] Writing Group of The Xiangya Expert Consensus on Liver Needle Biopsy. Writing group of the xiangya expert consensus on liver needle biopsy[J]. Chin J Gen Surg, 2021, 30( 1): 1- 8. DOI: 10.7659/j.issn.1005-6947.2021.01.001.肝脏穿刺活检湘雅专家共识编写组. 肝脏穿刺活检湘雅专家共识[J]. 中国普通外科杂志, 2021, 30( 1): 1- 8. DOI: 10.7659/j.issn.1005-6947.2021.01.001. [28] Clinical Guidelines Committee of Chinese Interventionalists College. Chinese clinical practice guidelines for transarterial chemoembolization of hepatocellular carcinoma[J]. Chin J Intern Med, 2021, 60( 7): 599- 614. DOI: 10.3760/cma.j.cn112137-20210425-00991.中国医师协会介入医师分会临床诊疗指南专委会. 中国肝细胞癌经动脉化疗栓塞(TACE)治疗临床实践指南(2021年版)[J]. 中华内科杂志, 2021, 60( 7): 599- 614. DOI: 10.3760/cma.j.cn112137-20210425-00991. [29] WANG GZ, HE XH, WANG Y, et al. Clinical practice guideline for image-guided multimode tumour ablation therapy in hepatic malignant tumours[J]. Curr Oncol, 2019, 26( 5): e658-e664. DOI: 10.3747/co.26.5423. [30] Chinese Society of Liver Cancer, China Anti-Cancer Association. Chinese expert consensus on hepatic arterial infusion chemotherapy for hepatocellular carcinoma(2021 edition)[J]. Chin J Dig Surg, 2021, 20( 7): 754- 759. DOI: 10.3760/cma.j.cn115610-20210618-00288.中国抗癌协会肝癌专业委员会. 肝动脉灌注化疗治疗肝细胞癌中国专家共识(2021版)[J]. 中华消化外科杂志, 2021, 20( 7): 754- 759. DOI: 10.3760/cma.j.cn115610-20210618-00288. [31] TRIPATHI D, STANLEY AJ, HAYES PC, et al. Transjugular intrahepatic portosystemic stent-shunt in the management of portal hypertension[J]. Gut, 2020, 69( 7): 1173- 1192. DOI: 10.1136/gutjnl-2019-320221. [32] Liver Failure and Artificial Liver Group, Chinese Society of Infectious Diseases, Chinese Medical Association; Severe Liver Disease and Artificial Liver Group, et al. Guideline for diagnosis and treatment of liver failure(2018)[J]. J Clin Hepatol, 2019, 35( 1): 38- 44. DOI: 10.3969/j.issn.1001-5256.2019.01.007.中华医学会感染病学分会肝衰竭与人工肝学组, 中华医学会肝病学分会重型肝病与人工肝学组. 肝衰竭诊治指南(2018年版)[J]. 临床肝胆病杂志, 2019, 35( 1): 38- 44. DOI: 10.3969/j.issn.1001-5256.2019.01.007. [33] Chinese Chapter of The International Hepato-Pancreato-Biliary Association; Group of Liver Surgery, Surgical Society of Chinese Medical Association; Expert Committee on Liver Cancer, Chinese Society of Clinical Oncology. Chinese multidisciplinary expert consensus on combined immunotherapy based on immune checkpoint inhibitors for hepatocellular carcinoma(2021 version)[J]. Chin J Hepatol, 2021, 29( 7): 636- 647. DOI: 10.3760/cma.j.cn501113-20210604-00261.国际肝胆胰协会中国分会, 中华医学会外科学分会肝脏外科学组, 中国临床肿瘤学会(CSCO)肝癌专家委员会. 基于免疫节点抑制剂的肝细胞癌免疫联合治疗多学科中国专家共识(2021版)[J]. 中华肝脏病杂志, 2021, 29( 7): 636- 647. DOI: 10.3760/cma.j.cn501113-20210604-00261. [34] Liver Cancer Committee of Chinese Medical Doctor Association. China expert consensus on clinical application of molecular targeted drugs for hepatocellular carcinoma(2020 edition)[J]. Natl Med J China, 2021, 101( 28): 2185- 2194. DOI: 10.3760/cma.j.cn112137-20210329-00760.中国医师协会肝癌专业委员会. 肝细胞癌分子靶向药物临床应用中国专家共识(2020版)[J]. 中华医学杂志, 2021, 101( 28): 2185- 2194. DOI: 10.3760/cma.j.cn112137-20210329-00760. [35] Cuidelines Working Committee of Chinese Society of Clinical Oncology. Chinese society of clinical oncology(CSCO). Guidelines of Chinese society of clinical oncology(CSCO) cancer therapy induced thrombocytopenia[M]. Beijing: People’s Medical Publishing House, 2022.中国临床肿瘤学会指南工作委员会组织. 中国临床肿瘤学会(CSCO)肿瘤治疗所致血小板减少症诊疗指南-2022[M]. 北京: 人民卫生出版社, 2022. [36] Nuclear Medicine Committee, Chinese Society of Clinical Oncology; Beijing Nuclear Medicine Quality Control and Improvement Center. Chinese expert consensus on selective internal radiation therapy with yttrium-90 for primary and metastatic hepatocellular carcinoma[J]. Chin J Hepatol, 2021, 29( 7): 648- 658. DOI: 10.3760/cma.j.cn501113-20210302-00103.中国临床肿瘤学会核医学专家委员会, 北京市核医学质量控制和改进中心. 钇-90( 90Y)微球选择性内放射治疗原发性和转移性肝癌的中国专家共识[J]. 中华肝脏病杂志, 2021, 29( 7): 648- 658. DOI: 10.3760/cma.j.cn501113-20210302-00103. [37] TERRAULT N, CHEN YC, IZUMI N, et al. Avatrombopag before procedures reduces need for platelet transfusion in patients with chronic liver disease and thrombocytopenia[J]. Gastroenterology, 2018, 155( 3): 705- 718. DOI: 10.1053/j.gastro.2018.05.025. [38] HUANG A, CHEN JF, WU JZ, et al. Effectiveness and safety of avatrombopag in liver cancer patients with severe thrombocytopenia: Real-world data and challenges[J]. J Oncol, 2022, 2022: 9138195. DOI: 10.1155/2022/9138195. [39] LI RX, YANG H, SONG YH, et al. Avatrombopag combined with intensive immune inhibition in the treatment of severe hepatitis-associated aplastic anemia: Report of two cases[J]. Chin J Pract Intern Med, 2021, 41( 12): 1086- 1088. DOI: 10.19538/j.nk2021120120.李瑞鑫, 杨慧, 宋玉华, 等. 阿伐曲泊帕联合强化免疫抑制治疗重型肝炎相关性再生障碍性贫血2例报告[J]. 中国实用内科杂志, 2021, 41( 12): 1086- 1088. DOI: 10.19538/j.nk2021120120. [40] LI RX, LIU ZY, ZHOU JT, et al. Avatrombopag in treatment of lenvatinib-related severe aplastic anemia: Report of one case and review of literature[J]. J Leuk Lymphoma, 2021, 30( 10): 618- 620. DOI: 10.3760/cma.j.cn115356-20210409-00078.李瑞鑫, 刘正媛, 周炯涛, 等. 阿伐曲泊帕治疗仑伐替尼相关重型再生障碍性贫血一例并文献复习[J]. 白血病·淋巴瘤, 2021, 30( 10): 618- 620. DOI: 10.3760/cma.j.cn115356-20210409-00078. [41] HIDAKA H, KUROSAKI M, TANAKA H, et al. Lusutrombopag reduces need for platelet transfusion in patients with thrombocytopenia undergoing invasive procedures[J]. Clin Gastroenterol Hepatol, 2019, 17( 6): 1192- 1200. DOI: 10.1016/j.cgh.2018.11.047. [42] DING ZB, WU H, ZENG YY, et al. Lusutrombopag for thrombocytopenia in Chinese patients with chronic liver disease undergoing invasive procedures[J]. Hepatol Int, 2023, 17( 1): 180- 189. DOI: 10.1007/s12072-022-10421-9. [43] KATSUBE T, WAJIMA T, FUKUHARA T, et al. Effects of food and calcium carbonate on the pharmacokinetics of lusutrombopag, a novel thrombopoietin receptor agonist[J]. Clin Ther, 2019, 41( 9): 1747- 1754.e 2. DOI: 10.1016/j.clinthera.2019.06.004. [44] AFDHAL NH, GIANNINI EG, TAYYAB G, et al. Eltrombopag before procedures in patients with cirrhosis and thrombocytopenia[J]. N Engl J Med, 2012, 367( 8): 716- 724. DOI: 10.1056/NEJMoa1110709. [45] HERMANN E, FERDJALLAH A. Eltrombopag-induced metabolic acidosis and hepatic encephalopathy in pediatric ITP[J]. J Pediatr Hematol Oncol, 2022, 44( 2): e453-e455. DOI: 10.1097/MPH.0000000000002300. [46] MOUSSA MM, MOWAFY N. Preoperative use of romiplostim in thrombocytopenic patients with chronic hepatitis C and liver cirrhosis[J]. J Gastroenterol Hepatol, 2013, 28( 2): 335- 341. DOI: 10.1111/j.1440-1746.2012.07246.x. [47] FENG R, LIU Y, ZHU XL, et al. Recombinant human thrombopoietin increases platelet count in severe thrombocytopenic patients with hepatitis B-related cirrhosis: Multicentre real-world observational study[J]. J Viral Hepat, 2022, 29( 5): 306- 316. DOI: 10.1111/jvh.13655. [48] DING JN, FENG TT, SUN W, et al. Recombinant human thrombopoietin treatment in patients with chronic liver disease-related thrombocytopenia undergoing invasive procedures: A retrospective study[J]. World J Gastrointest Surg, 2022, 14( 11): 1260- 1271. DOI: 10.4240/wjgs.v14.i11.1260. [49] LIU BW, XIANG HL, LIANG J, et al. Comparison of efficacy of recombinant human interleukin-11 and recombinant human thrombopoietin in treating thrombocytopenia with hypersplenism in cirrhotic patients[J]. World Chin J Dig, 2016, 24( 34): 4608- 4614. DOI: 10.11569/wcjd.v24.i34.4608.刘保文, 向慧玲, 梁静, 等. 重组人白介素-11及重组人血小板生成素在治疗肝硬化脾功能亢进所致血小板减少的疗效对比[J]. 世界华人消化杂志, 2016, 24( 34): 4608- 4614. DOI: 10.11569/wcjd.v24.i34.4608. [50] KUTER DJ. Treatment of chemotherapy-induced thrombocytopenia in patients with non-hematologic malignancies[J]. Haematologica, 2022, 107( 6): 1243- 1263. DOI: 10.3324/haematol.2021.279512. [51] Anti-Lymphoma Alliance in CSCO, Anti-Leukemia Alliance in CSCO, ASMC Group in CSCO, et al. China expert consensus on clinical application of recombinant human interleukin-11 in prevention and treatment of thrombocytopenia(2021 edition)[J]. Chin Clin Oncol, 2020, 25( 12): 1129- 1137. DOI: 10.3969/j.issn.1009-0460.2020.12.014.中国临床肿瘤学会抗淋巴瘤联盟, 中国临床肿瘤学会抗白血病联盟, 中国临床肿瘤学会抗肿瘤药物安全管理专家委员会, 等. 重组人白介素-11防治血小板减少症临床应用中国专家共识(2021年版)[J]. 临床肿瘤学杂志, 2020, 25( 12): 1129- 1137. DOI: 10.3969/j.issn.1009-0460.2020.12.014. [52] LIU L, LIU Y, GAO FY, et al. Clinical features of chronic liver disease with autoimmune blood diseases and the clinical effect of glucocorticoid[J]. J Clin Hepatol, 2021, 37( 8): 1878- 1882. DOI: 10.3969/j.issn.1001-5256.2021.08.025.刘龙, 刘遥, 高方媛, 等. 慢性肝病合并自身免疫性血液系统疾病的临床特征及应用糖皮质激素治疗效果分析[J]. 临床肝胆病杂志, 2021, 37( 8): 1878- 1882. DOI: 10.3969/j.issn.1001-5256.2021.08.025. [53] WU YY, LI HY, ZHANG TS, et al. Splanchnic vein thrombosis in liver cirrhosis after splenectomy or splenic artery embolization: A systematic review and meta-analysis[J]. Adv Ther, 2021, 38( 4): 1904- 1930. DOI: 10.1007/s12325-021-01652-7. [54] ZHAO P, LI T, XIE JL, et al. Value of early anticoagulant intervention in cirrhotic patients with portal hypertension after transjugular intrahepatic portosystemic stent shunt combined with PSE[J]. J Pract Hepatol, 2020, 23( 1): 82- 85. DOI: 10.3969/j.issn.1672-5069.2020.01.023.赵平, 黎涛, 谢吉良, 等. 早期抗凝干预用于经颈静脉肝内门体静脉支架分流术联合PSE治疗肝硬化患者价值探讨[J]. 实用肝脏病杂志, 2020, 23( 1): 82- 85. DOI: 10.3969/j.issn.1672-5069.2020.01.023. [55] FENG K, MA K, LIU Q, et al. Randomized clinical trial of splenic radiofrequency ablation versus splenectomy for severe hypersplenism[J]. Br J Surg, 2011, 98( 3): 354- 361. DOI: 10.1002/bjs.7367. [56] OGATA T, OKUDA K, SATO T, et al. Long-term outcome of splenectomy in advanced cirrhotic patients with hepatocellular carcinoma and thrombocytopenia[J]. Kurume Med J, 2013, 60( 2): 37- 45. DOI: 10.2739/kurumemedj.ms62010. [57] SHI XB, FENG JK, WANG JH, et al. Does splenectomy significantly improve the prognosis of hepatocellular carcinoma patients with hypersplenism? A systematic review and meta-analysis[J]. Ann Transl Med, 2021, 9( 8): 641. DOI: 10.21037/atm-20-6748. [58] CHU HB, HAN W, WANG L, et al. Long-term efficacy of subtotal splenectomy due to portal hypertension in cirrhotic patients[J]. BMC Surg, 2015, 15: 89. DOI: 10.1186/s12893-015-0077-2. [59] LIU X, QI XS, LI HY, et al. Prevalence of portal or splenic vein thrombosis in cirrhotic patients after splenectomy: A systematic review and meta-analysis of observational studies[J]. Int J Clin Exp Med, 2016, 9( 4): 7534- 7547. [60] TRIPODI A, PRIMIGNANI M, CHANTARANGKUL V, et al. Global hemostasis tests in patients with cirrhosis before and after prophylactic platelet transfusion[J]. Liver Int, 2013, 33( 3): 362- 367. DOI: 10.1111/liv.12038. [61] WANG SY, ZHOU WH, LI XY, et al. Analysis of platelet transfusion in liver disease patient[J]. J Clin Transfus Lab Med, 2017, 19( 4): 328- 331. DOI: 10.3969/j.issn.1671-2587.2017.04.005.王淑英, 周文辉, 李新颖, 等. 肝病患者血小板输注情况调查分析[J]. 临床输血与检验, 2017, 19( 4): 328- 331. DOI: 10.3969/j.issn.1671-2587.2017.04.005. [62] FURUICHI Y, TAKEUCHI H, YOSHIMASU Y, et al. Thrombopoietin receptor agonist is more effective than platelet transfusion for chronic liver disease with thrombocytopenia, shown by propensity score matching[J]. Hepatol Res, 2020, 50( 9): 1062- 1070. DOI: 10.1111/hepr.13530. [63] WEN LL, YU ZL, LIANG HL, et al. The main recommendation and enlightenment of application guidelines for platelet transfusion from British Society for Haematology[J]. Chin J Blood Transfus, 2018, 31( 4): 440- 444. DOI: 10.13303/j.cjbt.issn.1004-549x.2018.04.032.温丽玲, 余卓丽, 梁惠兰, 等. 英国血小板输注应用指南主要推荐及其启示[J]. 中国输血杂志, 2018, 31( 4): 440- 444. DOI: 10.13303/j.cjbt.issn.1004-549x.2018.04.032. [64] ZHU H, WANG SY, ZHU JH, et al. Efficacy and safety of transcatheter arterial chemoembolization combined with ginsenosides in hepatocellular carcinoma treatment[J]. Phytomedicine, 2021, 91: 153700. DOI: 10.1016/j.phymed.2021.153700. [65] NORONHA FERREIRA C, MARINHO RT, CORTEZ-PINTO H, et al. Incidence, predictive factors and clinical significance of development of portal vein thrombosis in cirrhosis: A prospective study[J]. Liver Int, 2019, 39( 8): 1459- 1467. DOI: 10.1111/liv.14121. [66] QI XS, DE STEFANO V, LI HY, et al. Anticoagulation for the treatment of portal vein thrombosis in liver cirrhosis: A systematic review and meta-analysis of observational studies[J]. Eur J Intern Med, 2015, 26( 1): 23- 29. DOI: 10.1016/j.ejim.2014.12.002. [67] LOFFREDO L, PASTORI D, FARCOMENI A, et al. Effects of anticoagulants in patients with cirrhosis and portal vein thrombosis: A systematic review and meta-analysis[J]. Gastroenterology, 2017, 153( 2): 480- 487.e 1. DOI: 10.1053/j.gastro.2017.04.042. [68] ZHOU T, SUN X, ZHOU T, et al. Efficacy and safety of nadroparin calcium-warfarin sequential anticoagulation in portal vein thrombosis in cirrhotic patients: A randomized controlled trial[J]. Clin Transl Gastroenterol, 2020, 11( 9): e00228. DOI: 10.14309/ctg.0000000000000228. [69] Hepatobiliary Disease Study Group, Chinese Society of Gastroenterology, Chinese Medical Association. Consensus for management of portal vein thrombosis in liver cirrhosis(2020,Shanghai)[J]. J Clin Hepatol, 2020, 36( 12): 2667- 2674. DOI: 10.3969/j.issn.1001-5256.2020.12.007.中华医学会消化病学分会肝胆疾病学组. 肝硬化门静脉血栓管理专家共识(2020年, 上海)[J]. 临床肝胆病杂志, 2020, 36( 12): 2667- 2674. DOI: 10.3969/j.issn.1001-5256.2020.12.007. [70] DECOUSUS H, TAPSON VF, BERGMANN JF, et al. Factors at admission associated with bleeding risk in medical patients: Findings from the IMPROVE investigators[J]. Chest, 2011, 139( 1): 69- 79. DOI: 10.1378/chest.09-3081. [71] KHANAL N, BOCIEK RG, CHEN BJ, et al. Venous thromboembolism in patients with hematologic malignancy and thrombocytopenia[J]. Am J Hematol, 2016, 91( 11): E468-E472. DOI: 10.1002/ajh.24526. [72] FALANGA A, LEADER A, AMBAGLIO C, et al. EHA guidelines on management of antithrombotic treatments in thrombocytopenic patients with cancer[J]. HemaSphere, 2022, 6( 8): e750. DOI: 10.1097/HS9.0000000000000750. 期刊类型引用(5)
1. 《中华消化外科杂志》编辑委员会. 血小板生成素受体激动剂在肝癌围手术期临床应用中国专家共识(2025版). 中华消化外科杂志. 2025(01): 21-30 .  百度学术
百度学术2. 任静,刘林,卢琴,杨国栋,汤善宏. 肝硬化患者血小板减少发生机制及功能变化分类的临床研究进展. 现代临床医学. 2025(02): 132-135 .  百度学术
百度学术3. 魏迅,秦新萌,马力,康谊. 阿伐曲泊帕治疗慢性肝病相关性血小板减少症临床疗效分析. 中国实用内科杂志. 2024(07): 567-570 .  百度学术
百度学术4. 王一婷. 荧光探针技术在疾病诊断中的最新进展. 中国卫生标准管理. 2024(17): 194-198 .  百度学术
百度学术5. 杨柏帅,梁立,严俊,袁敏. 部分性脾栓塞在肿瘤相关假性肝硬化所致血小板减少症患者中的应用. 中国中西医结合消化杂志. 2024(12): 1077-1081 .  百度学术
百度学术其他类型引用(1)
-




 PDF下载 ( 1405 KB)
PDF下载 ( 1405 KB)

 下载:
下载:



 下载:
下载:

 百度学术
百度学术